背景
开发人工智能(AI)和超声成像相结合,为胎儿心脏室间隔缺损(VSD)提供准确、客观、高效的辅助诊断方法。
方法
综合分析2016年1月至2022年6月期间500名孕妇的1451张胎儿心脏超声图像,由专家手工标记胎儿心脏区域并判别是否存在VSD。
训练集中遵循五重交叉验证的原则,开发AI模型来辅助VSD的诊断。使用 mAP@0.5、精度、召回率和 F1 分数等指标在测试集中评估模型。还比较了初级医生、中级医生和高级医生的诊断准确性和推理时间。
结果
AI模型诊断VSD的mAP@0.5、查准率、查全率和F1分分别为0.926、0.879、0.873和0.88。在该系统的辅助下,初级医生和中级医生的准确率分别提高了6.7%和2.8%。
结论
本研究报告了一种人工智能辅助的 VSD 诊断方法,与人工识别具有很高的一致性。它还具有较低的参数数量和计算复杂度,这也可以提高一些医生对VSD的诊断准确性和速度。
介绍
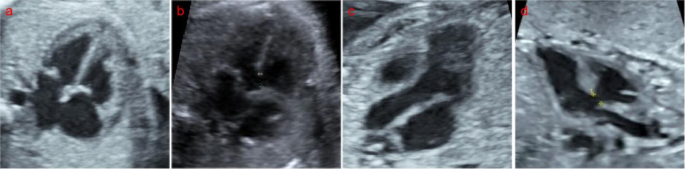
先天性心脏病(CHD)是新生儿死亡的原因之一,在我国,其发病率约占活产儿的4%~13%,全世界范围内,CHD的总发病率为0.8%~1.1%。1,2]。根据世界卫生组织(WHO)的资料,室间隔缺损(VSD)是冠心病的一种常见形式,是指心脏间隔部分发育不完全,导致心脏两个心室之间不完全分离。正常情况下,心脏的右心室和左心室被心室间隔分开,从而使循环中的富氧血液与贫氧血液分开。然而,VSD可能会导致这两种类型的血液混合,从而影响心脏的正常功能。据统计,VSD的患病率约为CHD的20%~57%[3]。许多研究表明,心尖四腔心脏切面(4CH)和左心室流出道切面(LVOT)是最常用的 VSD 产前筛查平面。4,5]。4CH和LVOT中VSD和no-VSD的示意图如图1所示。 1。VSD 缺损的宽度通常为 0.1 至 3.0 厘米,较小的缺损位于肌肉部分,较大的缺损位于膜部。小缺损时,心脏大小可以正常,但大缺损时,左心室比右心室扩大更明显。较大的缺陷不仅影响发育,而且还伴有进食困难、气短、出汗过多、乏力、呼吸困难、反复肺部感染,甚至伴有心力衰竭和感染性心内膜炎,严重影响孩子的健康。胎儿。VSD 可以单独存在,也可以与其他心脏异常(如房间隔缺损、动脉导管衰竭)同时存在,或作为心脏复杂异常的一部分(如永久性动脉干、法洛四联症和右心室双出口)。6,7]。由于本病与心腔内径变化和缺损大小密切相关,如果不及时干预,将会严重影响孩子的生长发育。此外,不同VSD胎儿的缺陷类型和部位不同,临床治疗时机的选择和预后评估也存在明显差异。因此,对于孕期患有VSD的胎儿,早期发现有助于及时识别缺陷的变化,明确其自愈的可能性,确保及时、有效的干预。这有利于母婴健康,显着改善预后,具有重要的临床意义。
随着现代科技的进步,利用产前超声筛查技术可以提高胎儿先心病的检出率。尽管3D/4D超声、多普勒超声和其他超声技术已经取得了很大进展,但2D超声由于其计算复杂度低且易于使用,仍然被广泛用作产前筛查工具。8]。然而,二维超声图像的解释对于超声医师来说是一项具有挑战性的任务。这是因为超声图像存在分散的噪声,导致图像的信噪比较低。阴影的影响也使得描绘潜在器官的边界变得困难。因此,器官的识别和异常的检测在很大程度上依赖于超声医师的专业知识,而先天性心脏病的诊断专业性很强,非专科医院医生的误诊和漏诊率很高。
机器学习和深度学习都是人工智能(AI)技术,主要通过模仿人脑中神经元的连接方式来处理复杂的任务。9]。人工智能在医学领域有着广泛的应用,如医学图像分析、病理和组织图像分析、基因组数据分析、疾病预测和监测等。8,10]。特别是在医学图像诊断方面取得了重大进展,可以从医学图像中提取复杂的特征来辅助医生进行疾病诊断和预测,例如通过深度卷积神经网络自动检测乳腺癌、肺癌等疾病网络(DCNN)[11,12]。许多研究表明,机器学习方法在胎儿产前筛查和出生风险预测中也很受欢迎[13,14,15]。许多学者应用机器学习模型来辅助医生预测胎儿出生窒息风险[16,17 号]。一些研究人员利用深度学习模型自动检测和定位胎儿的各种器官,如心脏、大脑、肺和四肢,这有助于医生更准确地评估胎儿的健康状况。18]。一些研究使用深度学习方法来监测胎儿生长趋势,包括测量头围、腹围和股骨长度等参数,这些信息对于评估胎儿发育是否正常至关重要。19]。一些学者还应用人工智能方法来检测和诊断可能的胎儿病变,例如心脏畸形、大脑异常、肾脏问题等。深度学习模型可以分析超声图像中的细节并提供早期诊断信息。20]。在本文中,我们应用AI方法辅助诊断胎儿心脏超声图像中的VSD,以提高诊断效率。
相关工作
近年来,人工智能(AI)在产科超声中的应用取得了显着进展,特别是在复杂胎儿结构检测、自动化图像分析、疾病筛查等方面。AI技术可显着提高产前超声的诊断效率和准确性。,并展示了专家级的检测水平,特别是在复杂的先天性心脏病 (CHD) 筛查方面。阿诺特等人。(2021)和 Ejaz 等人。(2024) 表明,人工智能可以通过多神经网络系统自动识别复杂的心脏结构,帮助医生减少误诊,特别是在新生儿先心病的早期筛查中。21,22 号]。Horgan 等人表示,人工智能在其他胎儿发育监测方面也显示出良好的效果。(2023) 以及 Ramirez Zegarra 和 Ghi (2023) 指出,人工智能可以通过自动化图像处理提高胎儿生长评估的准确性,并减少医生的工作量[23,24]。此外,5D超声成像技术与AI的结合为实时3D图像分析提供了更多维度信息,Jost等人。(2023)表明这种组合可能会彻底改变妇产科的临床实践[25]。在筛查胎儿心脑异常方面,Enache 等人。(2024)表明人工智能可以有效识别胎儿心脑结构异常,提高筛查效率并减少人工分析时间[26]。深度学习算法(例如卷积神经网络)在胎儿器官识别和疾病检测中的应用已经显示出其在图像分割和分析方面的优越性。27]。这些技术帮助人工智能在超声图像分析方面展现出巨大潜力。人工智能在妇产科领域的未来发展方向涵盖高危妊娠管理、早产预测等广泛领域。尽管其技术潜力巨大,但还需要进一步的临床验证和优化。马拉尼等人。(2023)表示,人工智能将继续通过自动化分析和深度学习支持医生进行更准确的诊断和风险评估[28]。孙树平等人。[29]利用心音时域和频域特征提取以及SVM分类器和椭圆模型成功诊断成人的小VSD、中度VSD和大VSD。陈世新等人。[30] 使用修改后的 YOLOv4-DenseNet 框架在多普勒超声图像上实现了成人三种 VSD 亚型的分类;刘嘉等人。[31] 使用残差卷积循环神经网络 (RCRnet) 分类模型分析了 884 名患有左向右分流冠状动脉疾病的儿童的心音记录,以实现房间隔缺损 (ASD)、室间隔缺损 (VSD)、动脉瘤周围导管的分类动脉供血不足 (PDA) 和合并冠状动脉疾病。三浦光太郎等人[32] 使用基于 CNN 的模型,在来自 2 大洲 3 家医院的 12 导联心电图上成功识别出 ASD 的存在;西蒂·努尔迈尼等人。[33】使用Mask-RCNN处理胎儿超声图像,对多个胎儿心脏结构实现了90%以上的分割检测精度;Lokaiah Pullagura 博士等人。[34】通过机器学习方法K-近邻算法和基于胎儿心电图(FECG)信号的决策树实现了胎儿先天性心脏病的识别。
本文的重点是开发一种基于人工智能和深度学习的模型,用于自动检测胎儿心脏超声图像中的室间隔缺损(VSD),并评估其辅助医生诊断的有效性。人工智能在动态超声视频中的有效性也得到了验证,展示了其实时临床应用的潜力。
材料和方法
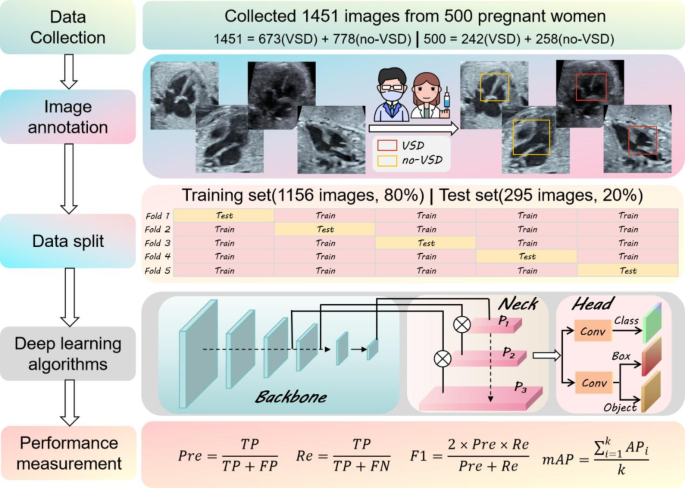
本研究的流程图如图所示。 2。我们首先回顾性收集孕妇的产前超声筛查记录,获得符合要求的胎儿心脏超声图像。然后,对胎儿心脏的间隔区域进行标记,并由专家对是否存在 VSD 进行分类。基于原始图像和标记信息,遵循五重交叉验证的原则,在训练集和测试集上对深度学习胎心VSD检测算法进行训练和评估。最后对其性能进行了总结和报告。
患者特征
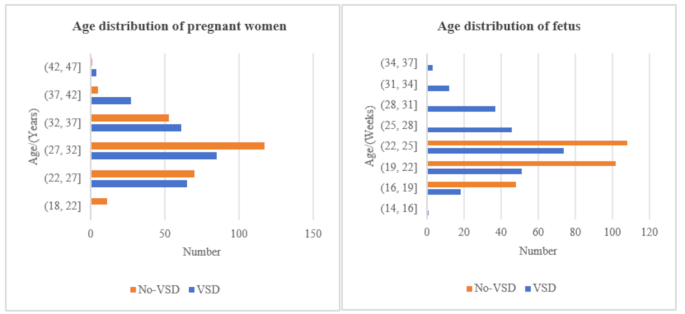
在回顾性研究中,选取2016年1月至2022年6月期间在福建医科大学第一医院和福建医科大学第二医院接受产前胎儿心脏超声检查的500名孕妇进行研究。孕妇平均年龄为30岁,最大值为46岁,最小值为18岁;平均孕周为22周,最大值为39周±6天,最小值为14周±3天,如表所示。 1。孕妇及胎儿的年龄分布如图1所示。 3。从产妇年龄分布图中可以看出,年龄分布通常并不正常。具体来说,孕妇的年龄高度集中在27-32岁区间,其他区间分布较少。这表明母亲年龄的数据可能存在偏差,因此使用中位数更为合适。孕周分布图也表现出一定的集中性,尤其是VSD组孕周大多集中在22周至28周之间,而无VSD组孕周分布较宽。基于这些分布特征,胎龄的数据也可能存在偏差,因此还应该采用中位数来更准确地反映胎龄的分布情况。其中,242 名诊断为 VSD 的胎儿有金标准心血管血管造影和/或手术结果作为验证。所有患者均签署书面知情同意书,所有数据均匿名。
图像采集
我们获得了500名孕妇的1451张胎儿心脏超声图像,检查所使用的仪器有DC-8、Resona 8(中国迈瑞)、Voluson E10、Voluson E8、Voluson E6、Rietta 70、HI Vision Preiru、二郎神(日本日立)、Logiq P6、Expert 730(美国通用电气)、Aixlorer(声学、法国)和 Sequoia 512(德国西门子)。图像尺寸为 704–561、720–576、720–370、768–576 和 1260–576Ø910。超声图像的纳入标准如下: (1)图像不包含多普勒信号。(2) 未观察到过多的声影。(3) 如果同一孕妇在系统中记录了多次检查,则每次检查之间的间隔将超过四个星期。(4) 基于关键心脏标志的清晰可见度,图像被认为适合选择。具体来说,四腔视图(4CH)清楚地显示了左右心房和心室的结构,重点是室间隔的连续性。左心室流出道(LVOT)视图清楚地显示主动脉瓣和左心室流出道的解剖结构,特别强调室间隔和主动脉根部之间的关系。
图像标注
所有 2D 超声图像均由两位经验丰富的超声医师使用标记软件 labelme 进行标记。为了进行注释,需要一名超声医师在胎儿心脏超声图像中手动勾勒出室间隔的范围。另一位超声医师审查所有手动注释,以确保注释的质量,对于任何分歧,两位专家根据需要进行讨论并提出新的注释,直到达成共识。这是开发和验证深度学习算法的重要事实。
深度学习算法
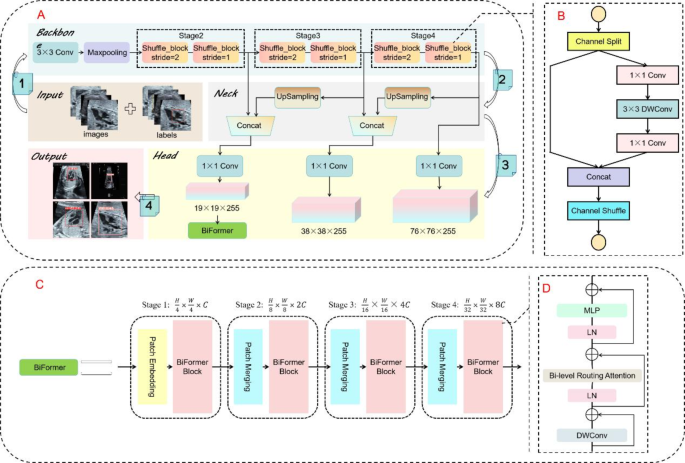
在这项工作中,我们设计了一个端到端的深度学习模型来检测 VSD。我们根据真实的诊断结果分别用 0 和 1 标记我们的数据,其中 1 代表存在 VSD,0 代表不存在。我们设计的监督网络检测所有图像的心室间隔区域,并在真实标签的指导下将它们分类为 0 和 1。网络结构由四个模块组成:Input、Backbone、Neck、Head,如图所示。 3(一个)。胎心超声图像在输入部分经过数据增强等一系列操作进行预处理,然后输入骨干网络,骨干网络从处理后的图像中提取部分特征;随后,提取的特征通过Neck模块进行融合,得到大、中、小三种尺寸的特征;融合后的特征输入Head模块,Head模块检测后输出室间隔区域的定位结果以及有无VSD的分类结果。
本工作中的整个网络可以描述为类似于YOLOv5的网络,如图所示。 4(A),但有两部分不同。首先是Backbone的网络结构,我们设计了Backbone,其中基于Group Convolution和Channel Shuffle这两个关键技术使用了Shuffle_block,在保持高性能的同时显着降低了计算复杂度和参数数量,如图所示。一个 4(二)。主要思想是将输入通道分为多个组。然后重新排列这些通道,以便每个组包含来自不同输入通道的信息,然后在每个组内执行卷积运算。其次,我们在Head模块的小目标输出层添加基于两层路由的动态稀疏注意力机制,以实现更灵活的计算分配和内容感知,如图2所示。 4(三)。基于所提出的两层路由注意力,我们还提出了一种新的通用视觉转换器,称为 BiFormer,如图 1 所示。 4(四)。它利用稀疏性来节省计算量和内存,并且仅涉及 GPU 友好的密集矩阵乘法,仅关注相关区域的一小部分,而不会受到其他不相关区域的干扰,从而获得出色的性能和计算效率,尤其是在密集预测任务中,例如,胎儿心脏隔膜,一种小而致密的结构。与其他模型的比较表明,我们的模型比基准模型的复杂度低得多,并且模型参数的数量大大减少。
培训策略
为了解决正负样本大小不平衡的问题,我们使用Mosaic数据增强方法,在每个训练批次中随机选择四张不同的图像,随机选择一个合成位置,并在选定的合成位置将四张图像拼接在一起形成新的合成图像。这个合成过程涉及缩放、裁剪和将四个图像排列在一起,以便它们形成一个完整的图像。目标的标签信息也被调整,目标边界框的坐标和尺寸被重新计算并映射到新的合成图像上。这提高了模型的泛化能力,帮助模型更好地处理复杂场景,提高模型的鲁棒性。同时,我们在训练过程中遵循五重交叉验证的原则对数据集进行划分,以确保模型在多个不同的训练集和测试集上进行评估,从而提高模型的稳定性和泛化性。
实验在运行 Windows 10 的计算机上进行,硬件配置如下:CPU 为第 12 代 Intel(R) Core (TM) i5-12400F,RAM 为 16GB,GPU 内存为 NVIDIA GeForce RTX3050。使用的编程环境是Python 3.8。实验中使用的深度学习框架是Pytorch 1.9。实验过程将所有图像按照8:2的比例分为训练集和测试集。输入图像的尺寸均为640××640,训练进行300个epoch。数据集划分详细信息如表所示 2。表2 数据集划分在本研究中,对所提出的深度学习架构进行超参数调整,以确保最佳模型性能。
为了找到最佳模型,我们采用实验性试错方法,通过试验多个超参数组合并测试它们在验证集上的性能。经过多次实验和调整,我们最终选择了以下超参数设置:学习率为0.01,批量大小为8,并使用SGD优化器进行训练。每个实验的结果均通过mAP@0.5、精度、召回率、F1分数等指标进行五重交叉验证,最终确定当前最优模型配置。
性能测试
通过 5 倍交叉验证检测 mAP@0.5、精度 (Pre)、召回率 (Re) 和 F1 分数来定量评估模型。
精度是模型预测为正例的样本与实际为正例的样本的比例。它由以下公式表示:
$$\:\begin{array}{c}Pre=\frac{TP}{TP+FP}\end{array}$$
(1)
其中TP(True Positives)表示模型正确预测为正例的样本数,FP(False Positives)表示模型错误预测为正例的样本数。精度越高表明模型对阳性病例的预测越准确。
召回率是模型成功预测为阳性的真正阳性样本的比例。它由以下公式表示:
$$\:\begin{array}{c}Re=\frac{TP}{TP+FN}\end{array}$$
(2)
其中TP(True Positives)表示模型正确预测为正例的样本数量,FN(False Negatives)表示模型错误预测为负例的样本数量。高召回率表明模型更好地捕获了正面示例。
F1 分数是精确率和召回率的调和平均值,它结合了模型的准确率和覆盖率。F1分数由以下等式表示:
$$\:\begin{array}{c}F1=\frac{2\times\:Precision\times\:Recall}{Precision+Recall}\end{array}$$
(3)
F1 分数取 0 到 1 之间的值,其中 1 表示性能最佳,0 表示性能最差。
mAP 综合不同类别的精确召回曲线并计算它们的平均值。mAP计算通常包括以下步骤:
-
(1)
计算每个类别的精确率-召回率曲线。
-
(2)
计算每个类别的曲线下面积 (AUC)。
-
(3)
对所有类别的 AUC 进行平均以获得 mAP。
mAP的取值范围为0到1,其中1表示性能最好,0表示性能最差。在本研究中,我们使用mAP@0.5作为评估指标,其中0.5意味着我们将IoU(Intersection over Union)阈值设置为0.5。这意味着当预测帧与真实帧的IoU大于或等于0.5时,认为检测是正确的。这种选择基于目标检测任务的标准实践,可以平衡检测的准确性和召回率,而不会增加太多误报。我们相信mAP@0.5可以有效反映AI模型在检测VSD方面的整体性能,并有助于衡量其在复杂临床应用中的稳健性。
为了充分评估我们模型的性能,我们将其与当前性能更好的分类模型(Resnet18 [35]�EfficientnetV2s [36] 密集网 [37] 移动网V3-大[38])以及目标检测模型(Faster R-CNN [39]�YOLOV5s [40]�YOLOV7 [41]�YOLOX [42])。
统计分析
采用SPSS 20.0软件进行统计分析,并采用McNemar’s检验评估不同模型的性能。当p值小于0.05时,表明差异具有统计显着性。
结果
在我们的检测任务中,VSD 被视为主要检测类别。No-VSD 不被视为单独的检测类别,而是意味着给定图像中不存在 VSD。如果既没有检测到 VSD 也没有检测到非 VSD,图像将被归类为“未检测到”,这意味着模型没有识别任何相关的分类特征。这种方法确保重点仍然是识别 VSD 的存在,而不会因不相关或不明确的检测而引入额外的复杂性。
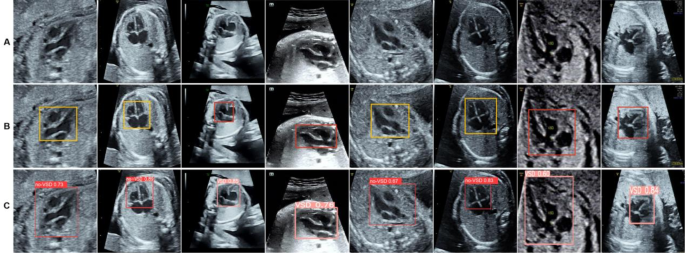
VSD模型的实时检测结果如图1所示。 5。其中A行是原始图像,B行是专家标注,C行是模型的检测结果;第一列和第五列是 LVOT 中的无 VSD,第二列和第六列是 4CH 中的无 VSD,第三列和第八列是 4CH 中的 VSD,第四列和第七列是 LVOT 中的 VSD。结果表明,深度学习方法对于胎儿心脏室间隔区域的检测以及VSD的自动诊断与人工判别具有高度的一致性。
除了静态超声图像的分析之外,我们还在动态筛查视频上测试了 AI 模型。通过分析捕获的实时超声视频,进一步验证了AI模型在动态检测方面的性能。胎心超声筛查AI模型的视频检测效果如图:https://github.com/1024Strawberry/VSD。图5
表
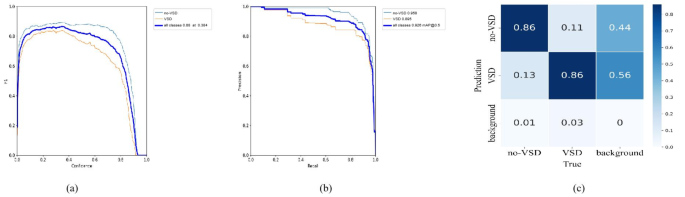
3显示 5 倍交叉验证的结果。第四折具有最高的训练评估指标,保存模型权重以供后续测试。该模型的平均 mAP@0.5 为 0.91,平均精度为 0.855,平均召回率为 0.883。单个指标可以在单次训练验证运行中重现。图 6显示了从用于测试集的第四次折叠获得的模型权重的结果。
比较结果
表 4显示了与现有分类和目标检测模型在胎心超声图像中辅助诊断 VSD 的性能比较结果。在本研究中与 AI 模型进行比较的模型中,ResNet50、EfficientNetV2s、DenseNet201 和 MobileNetV3-large 是在 ImageNet 数据集(广泛用于图像分类任务的公共数据集)上进行预训练的。相比之下,目标检测模型Faster R-CNN、YOLOv5s、YOLOv7和YOLOX-s通常使用COCO或ImageNet数据集进行预训练。这些预训练使模型为广泛的图像分类和检测任务做好了准备。另一方面,我们的模型专门在胎儿心脏超声图像数据集上进行训练,并且没有使用公开可用的数据集进行预训练,从而使其更好地适应医学图像的特定需求。“参数”和“FLOPS”用于衡量模型的复杂性和计算效率。具体来说,“参数”的数量表示模型中可训练参数的数量,“参数”数量越少意味着模型更轻量级,适合在计算资源有限的环境中运行。FLOPS用来衡量模型运行所需的计算量,表示模型每秒执行的浮点运算次数。通过分析这两个指标,我们可以评估模型在不同硬件设备上的性能,以确保其能够在资源受限的设备上高效运行,同时保持高精度。本研究选择的模型参数数量和FLOPS值较低,特别适合部署在资源匮乏的环境中,具有较高的检测性能。我们使用的方法可以在保持高性能的同时减少计算和存储开销,并且更适合适用于设备算力较低的资源受限环境。
表 5显示了我们的方法与初级医生、中级医生和高级医生对胎儿心脏超声图像的 VSD 诊断结果的比较。具体来说,初级医生是指经验较短(通常为1~2年)、正处于专业知识和技能积累阶段的医生。高级医生是指工作经验较长(一般在10年以上)、具有丰富的临床诊断经验、能够独立处理复杂病例的医生。可以看出,我们的方法的诊断精度与资深医生相同,但一张图像的推理速度的单位级别从分钟提高到毫秒;同时,在AI方法的辅助下,初级医生和中级医生的诊断准确率分别提高了6.7%和2.8%。
结论与讨论
在这项研究中,我们基于胎儿心脏超声图像对 VSD 进行了探索。我们提出了一种人工智能方法,该方法已经在两家医院的 1451 张胎儿心脏超声图像上进行了训练和测试。经验证,我们的模型参数数量少,计算复杂度低,识别VSD存在的准确率达到92.6%,与资深医生的诊断结果高度一致,速度提升至7ms/张,对初级医生的诊断有一定的辅助作用。同时,我们的方法的性能优于其他分类模型和目标检测模型,并且更适合资源有限和设备运算量较低的区域。
本研究表明,人工智能模型在辅助医生进行VSD诊断方面具有显着效果,特别是在提高初级和中级医生的诊断准确性方面,这对医学教育和临床培训具有重要意义。传统的医疗培训依赖于大量病例和经验的积累,初学者在诊断小型复杂的VSD时常常会遇到困难。AI系统能够通过自动识别和注释技术实时提供即时反馈,帮助医生识别更快、更准确地识别心脏结构和异常,尤其是在复杂或罕见的情况下,人工智能的帮助弥补了经验不足的缺点。将人工智能系统融入医疗培训中,可以为初学者提供交互式学习平台,生成高精度的诊断结果,持续跟踪医生的诊断决策,帮助医生了解并改进诊断过程中的弱点,从而提高医疗技能的掌握。通过长期使用,医生不仅可以提高VSD诊断能力,还可以通过与AI的互动学习,提高整体图像判读和心脏病学知识,缩短学习曲线。此外,AI系统还可以作为资源有限地区的远程学习工具,帮助年轻医生在没有专家指导的情况下获得高质量的诊断反馈,提供标准化的诊断支持,有助于减少医生之间的差异。医生之间的诊断水平,促进医学教育的普及和公平。
然而,这项研究仍然存在一些局限性。首先,我们认识到本研究仅证实了少数 VSD 类型,例如膜性和肌肉性 VSD。由于VSD可以发生在隔膜的任何位置,甚至可能发生多个VSD,未来的研究将考虑纳入更多的VSD类型和复杂的病例,以提高AI模型的适应性。其次,本研究中的 AI 模型训练和测试基于静态超声图像,未在临床实时视频循环或胎儿扫描中进行评估。我们意识到这可能与实际的临床筛查环境存在差距,特别是对于初学者来说,检测小 VSD 很困难。因此,未来的研究将重点关注AI系统在实时动态扫描中的应用,并评估其在不同胎位、无彩色多普勒等不利条件下的性能。第三,这项研究最初验证了AI在静态图像中的诊断功效,但仍有必要在实际临床环境中测试其可行性,尤其是在实时筛查中。未来的前瞻性研究将进一步评估AI在实时超声扫描中VSD检测率的增强,并探索其在实际诊断中的潜在临床应用值。最后,由于深度学习模型的黑盒性质,VSD诊断中间过程的可解释性很低。未来的研究应旨在提高模型的准确性和可靠性,以便能够在早期阶段检测和分类不同类型的心脏缺陷。也可以将不同的医学图像方式以及临床数据组合在一起,从而可以对先天性心脏病进行更全面的评估和诊断。应该更多地关注如何解释模型的决策并提供可靠的不确定性估计,以帮助医生了解诊断结果。
数据可用性
当前研究期间使用和/或分析的数据集可根据合理要求从相应作者处获得。为了验证AI系统在动态超声筛选中的性能,包括与实时筛选视频的链接,供读者进一步查看测试过程和结果。(https://github.com/1024 strawberries/vsd)
缩写
- 冠心:
-
先天性心脏病
- VSD:
-
室间隔缺损
- 4CH:
-
四腔心脏视图
- LVOT:
-
左心室流出道视图
- DCNN:
-
深度卷积神经网络
- 人工智能:
-
人工智能
参考
El-Chouli M,Mohr GH,Bang CN,Malmborg M,Ahlehoff O,Torp-Pedersen C,Gerds TA,IDORN L,RAUNSTH J,GISLASON G。。J Am 心脏协会。2021; 10(14):E020375。EPUB 2021年7月3日。34219468;PMCID:PMC8483486。
Pan F,Xu W,Li J,Huang Z,Shu Q.过去三十年来,中国先天性心脏病负担的趋势。浙江大学学报一学班。2022; 51(3):267 77。https://doi.org/10.3724/zdxbyxb-2022-0072。英语。
世卫组织共同世界卫生组织。响应Covid-19参考的社区传播WHO/covid-19/community_transmission/20201。2020.
Rieder W,Eperon I,Meagher S.先天性心脏异常在妊娠中期:从筛查到诊断。普雷纳特诊断。2023; 43:889 900。
Tudorache S,Cara M,Iliescu DG,Novac L,Cernea N.头三个月和四维心脏扫描:内部和观察者间的一致性,颜色多普勒技术的方法和益处之间的比较。超声产科妇科。2013; 42:659 68。
Soto B,Becker A,Moulaert A,Lie J,Anderson R.心室间隔缺陷的分类。心。1980; 43:332â43。
Penny DJ,Vick GW。室间隔缺损。柳叶刀。2011; 377:1103 12。
Sridevi S,Kanimozhi T,Bhattacharjee S,Reddy SS,ShahwarD。从超声图像中对产前心室中文缺陷的杂交量子经典神经网络分类。在:国际计算智能与数据工程会议上。施普林格;2022.pp。461 - 8。
Lecun Y,Bengio Y,Hinton G.深度学习。自然。2015; 521:436 44。
Ximenes RS,Bravo-Valenzuela NJ,Pares DBS,AraujoJãºNiorE。在先天性心脏病的第一久产前诊断中使用心脏超声成像。J 临床超声。2023; 51:225 39。
Amrane M,Oukid S,Gagaoua I,Ensari T.使用机器学习的乳腺癌分类。2018电气电子,计算机科学,生物医学工程会议(EBBT)。IEEE;2018。第1页。
Wang D,Khosla A,Gargeya R,Irshad H,Beck AH。深度学习,以识别转移性乳腺癌。ARXIV预印型ARXIV:160605718。2016年。
Horgan R,Nehme L,Abuhamad A.产科超声中的人工智能:范围评论。普雷纳特诊断。2023 年。
Darsareh F,Ranjbar A,Farashah MV,Mehrnoush V,Shekari M,Jahromi MS。机器学习的应用来识别出生窒息的危险因素。BMC 怀孕分娩。2023; 23:156。
Huang B,Zheng S,Ma B,Yang Y,Zhang S,Jin L.使用深度学习来预测10,000多个胚胎数据的活产结果。BMC 怀孕分娩。2022; 22:36。
MN,Mustafina SN,Mahmud T,Khan Ni。用于预测怀孕结果的机器学习:系统评价,综合框架和未来的研究议程。BMC 怀孕分娩。2022; 22:348。
Gangadhar MS,Sai KVS,Kumar SHS,Kumar KA,Kavitha M,Aravinth S.机器学习和深度学习技术,涉及冠心病的准确风险预测。在:,方法论,交流。(ICCMC)。IEEE;2023。pp。227â32。
莫里斯·萨(Morris SA),洛佩兹(Lopez KN)。深度学习用于检测胎儿先天性心脏病。纳特医学。2021; 27:764 - 5。
Wang Y,Shi Y,Zhang C,Su K,Hu Y,Chen L等。基于深神网络的胎儿体重估计:回顾性观察性研究。BMC 怀孕分娩。2023; 23:560。
Zhu J,Chen J,Zhang Y,JiJ。先天间隔缺陷的新生儿的脑组织发育:深度学习算法的MRI图像评估研究。巴基斯坦医学科学杂志。2021; 37:1652。
谷歌学术一个
Arnaout R,Curran L,Zhao Y,Levine JC,Chinn E,Moon-Grady AJ。神经网络的合奏提供了复杂先天性心脏病的专家级产前检测。纳特医学。2021; 27(5):882â91。
Ejaz H,Thyyib T,Ibrahim A,Nishat A,MalayJ。人工智能在早期发现新生儿的先天性心脏病中的作用。前面的数字健康。2024; 5:1345814。
Horgan R,Nehme L,Abuhamad A.产科超声中的人工智能:范围评论。普雷纳特诊断。2023; 43(9):1176 219。
Ramirez Zegarra R,Ghi T.在胎儿超声成像中使用人工智能和深度学习。超声产科妇科。2023; 62(2):185 94。
Jost E,Kosian P,Jimenez Cruz J,Albarqouni S,Gembruch U,Strizek B,Recker F.不断发展5D超声的时代?关于人工智能应用超声成像在妇产科中的超声成像的系统文献综述。临床医学杂志。2023; 12(21):6833。
Enache,I。A.,Iovoaica-räMescu,C.,Ciobanu,è。G.,Berbecaru,E。I. A.,Vochin,A。产科异常扫描中的人工智能:心脏和大脑。生活,14(2),166。
Fiorentino MC,Villani FP,DI Cosmo M,Frontoni E,MocciaS。胎儿超声图像分析的深度学习算法的综述。Med图像肛门。2023; 83:102629。
Malani IV,Shrivastava SN,D.,Raka MS。(2023)。对人工智能在妇产科中的作用的全面回顾。Cureus,15(2)。
Sun S,Wang H,Jiang Z,Fang Y,TaoT。基于分割的心脏声音提取与VSD诊断系统的分类器模型相结合。专家系统应用2014; 41:1769 80。
Chen S-H,Tai I-H,Chen Y-H,Weng K-P,Hsieh K-S。用于心室缺陷超声图像分类的深度学习框架的数据增强。SpringerLink。2021;:310 22。
Liu J,Wang H,Yang Z,Quan J,Liu L,TianJ。基于学习的基于学习的计算机辅助心脏声音分析,患有右右流先天性心脏病的儿童。国际心脏杂志。2022; 348:58 64。
Miura K,Yagi R,Miyama H,Kimura M,Kanazawa H,Hashimoto M等。基于深度学习的模型检测心电图学中的间隔缺陷:横断面多中心基于医院的研究。Eclinicalmedicine。2023 年。
Nurmaini S,Rachmatullah MN,Sapitri AI,Darmawahyuni A,Jovandy A,Firdaus F等。使用基于深度学习的多类实例分割的胎儿超声图像准确检测中间缺陷。IEEE 访问。2020; 8:196160 74。
Lokaiah Pullagura MRD博士。通过机器学习技术识别胎儿心脏病。Annals RSCB。2021; 25:2601 15。
谷歌学术一个
何凯,张旭,任胜,孙静。图像识别的深度残差学习。见:IEEE 计算机视觉和模式识别会议论文集。2016。第770页8。
Tan M,Le Q.有效NETV2:较小的型号和更快的训练。见:机器学习国际会议。PMLR;2021。pp。10096106。
Iandola F,Moskewicz M,Karayev S,Girshick R,Darrell T,Keutzer K. Densenet:实施有效的Convnet描述符金字塔。ARXIV预印型ARXIV:14041869。2014年。
Howard A,Sandler M,Chu G,Chen L-C,Chen B,Tan M等。正在搜索 mobilenetv3。见:IEEE/CVF 计算机视觉国际会议论文集。2019。第1314页。24。
Ren S,He K,Girshick R,Sun J.更快的R-CNN:使用区域提案网络实时检测。高级神经信息处理系统。2015; 28。
Jocher G,Chaurasia A,Stoken A,Borovec J,Kwon Y,Michael K等。Ultrytics/Yolov5:V6。2-Yolov5分类模型,Apple M1,可重复性,ClearML和DECI。AI集成。泽诺多.2022 年。
王长云,博赫科夫斯基 A,廖 H-YM。YOLOV7:可训练的释放袋为实时对象探测器设定了新的最新最先进。2023 年。
Ge Z,Liu S,Wang F,Li Z,Sun J. Yolox:2021年超过Yolo系列。Arxiv预印型Arxiv:210708430。2021 年。
致谢
作者要感谢帮助收集和标记数据的护士和医生。作者要对BMC怀孕和分娩的编辑和审稿人表示衷心的感谢,他们对这项研究的宝贵评论和建议。在手稿的修订和完善过程中,编辑人员的专业指导以及审稿人的建设性反馈大大提高了本文的质量和严谨性。我们对他们的辛勤工作和支持表示衷心的感谢。
资金
这项工作得到了福建国家自然科学基金会(2021J011404,2023J01173,2023J011784)和Quanzhou Scientific and Technological Planning项目(20222NS057)的支持。
道德声明
道德批准并同意参与
这项研究符合赫尔辛基在涉及人类受试者的医学研究上宣布的。所有患者均签署了书面知情同意书,并在我们的中心接受了常规临床治疗。它得到了福建医科大学第二附属医院的医疗伦理委员会(2020年115年)的批准。
同意发表
不适用。
利益竞争
作者声明没有竞争利益。
附加信息
出版商备注
施普林格·自然对于已出版的地图和机构隶属关系中的管辖权主张保持中立。
电子补充材料
以下是电子补充材料的链接。
权利和权限
开放获取本文获得 Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License 的许可,该许可允许以任何媒介或格式进行任何非商业使用、共享、分发和复制,只要您给予原作者适当的署名即可和来源,提供知识共享许可的链接,并指出您是否修改了许可材料。根据本许可,您无权共享源自本文或其部分内容的改编材料。本文中的图像或其他第三方材料包含在文章的知识共享许可中,除非材料的出处中另有说明。如果文章的知识共享许可中未包含材料,并且您的预期用途不受法律法规允许或超出了允许的用途,则您需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by-nc-nd/4.0/。转载和许可
引用这篇文章
Li,F.,Li,P.,Liu,Z。
等人。在胎儿心脏超声图像中,在VSD产前诊断中应用人工智能。BMC 怀孕分娩24 ,758(2024)。https://doi.org/10.1186/s12884-024-06916-y
已收到:
公认:
已发表:
DOI:https://doi.org/10.1186/s12884-024-06916-y