
人工智能工具学会逐片段构建分子
作者:Alexander Whiteside
用于药物设计的新机器学习工具通过巧妙处理分子几何形状提出更好、更现实的药物。FragGen 软件逐个片段地构建分子,并针对每个决策使用不同的机器学习过程,以最大程度地减少每个决策的固有缺点。FragGen 的创建者能够选择抗癌靶点、设计新药、合成新药并通过实验证明其效力。
许多药物通过与蛋白质中的特定口袋结合来发挥作用。与其靶标牢固结合的药物往往更有效。机器学习方法应该能够学习这些目标的结构与善于结合它们的分子的质量之间的关系。然而,与所有分子和所有蛋白质口袋的空间相比,可用于教学模型的示例数量很少,因此药物发明的预言尚未出现。一些模型可能提出化学上不合理的原子排列,而另一些模型可能提出具有大量稠合芳环的分子,这些分子在化学上是合理的,具有很强的结合力,但不像药物并且难以合成。
通过从碎片中逐个构建分子,可以更容易地形成化学上敏感的结构。” 以前基于结构的分子生成方法基本上学习如何与分子紧密结合,通常通过训练隐式了解真实的、可合成的分子是什么样子,”解释道张奥丁中国浙江大学博士,FragGen 的创建者之一。– 基于构建块设计分子迫使分子生成路径是可合成的。 – 然而,这种方法的逐步性质意味着每个片段的放置中的任何错误都会累积,因此分子可能会扭曲成一个令人难以置信的结构装订袋中的几何形状。
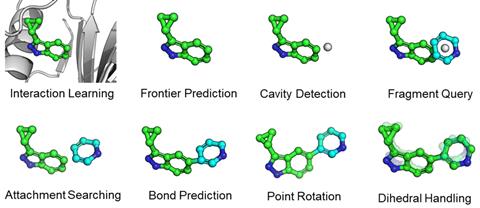
FragGen 是一种基于片段的方法,通过以非常谨慎的方式处理分子的几何形状来强加顺序。从空口袋开始,一个机器学习模型决定应将新片段添加到哪个原子;另一个片段应该是什么;另一个它应该如何与目标原子结合;等等几何变量,如键角和二面角。它使用已知适合此类预测的不同模型来解决每个较小的问题。
将问题分解为一系列可以通过更简单的模型来解决的步骤是“设计以深思熟虑的方式使用深度学习的科学工具的一种非常好的方法”,他说雷·曼斯巴赫,加拿大康考迪亚大学计算生物物理学家。“我认为人们对这样的想法感到非常兴奋:只需将数据放入其中,它就会产生某种模型,但我认为这不一定是最有效的方法”。
FragGen 的药物建议在许多关于效力和合成简易性的常见理论测量方面得分很高。更重要的是,它们通过了实验测试。研究人员使用 FragGen 设计了一种 II 型激酶抑制剂。该软件在短短 10 分钟内推荐了 97 种候选药物,其中三种最有利的候选药物被发现在微摩尔和纳摩尔浓度下既可合成又有效。
为了安全起见,药物还必须对结合袋具有特异性,并且不能与其他重要蛋白质结合并影响其他重要蛋白质。FragGen 等工具尚无法做到这一点,但它们在发现过程中提供了一个有价值的起点。“你想要应用人工智能和深度学习方法的地方通常是在设计之初,这样你就可以扫描空间,寻找你没有想到的东西,并将搜索范围缩小到可管理的范围,”曼斯巴赫说。
