一种使用机器学习算法和可解释的人工智能方法预测心脏病的技术方案
作者:El-Latif, Yasser M. Abd
介绍
全球范围内,心脏病一直是导致死亡的主要原因1根据世界卫生组织的报告,心脏病和中风每年在全球造成1750万例死亡。超过75%的心脏病死亡发生在中低收入国家。此外,心脏病发作和中风导致了所有心血管疾病致死案例中的80%。2观察患者的症状并进行体格检查通常可以诊断出心脏病。吸烟、年龄、家族心脏疾病史、高胆固醇水平、缺乏运动、高血压、肥胖、糖尿病和压力是心血管疾病的某些风险因素。3生活方式的改变,如戒烟、减肥、运动和管理压力,可能有助于减少这些风险因素。我们通过病史采集、体格检查以及心电图、超声心动图、心脏磁共振成像和血液检测等影像学检查来诊断心脏病。生活方式的调整、药物治疗以及诸如血管成形术、冠状动脉旁路移植手术或植入式设备(如起搏器或除颤器)等医疗手段可以治疗心脏病4现在可以通过利用越来越多的医疗系统所提供的易于获取的大量患者数据来构建心脏病预测模型。机器学习被认为是一种数据分析方法,它从多个角度分析大规模的数据集,然后将结果转化为切实的知识。5.
几项研究利用了如支持向量机(SVM)、人工神经网络(ANN)、决策树(DT)、逻辑回归(LR)和随机森林(RF)等机器学习算法来分析医疗数据并预测心脏病。一项最近的研究由6使用机器学习模型预测多族裔人群的心脏病风险。作者利用了大量电子健康记录数据,并将其与社会人口统计信息关联起来,以划分心血管疾病的风险等级。这些模型在预测多族裔人群中心血管疾病的高风险方面取得了很高的准确性。同样,另一项研究也表明7应用深度学习(DL)算法预测冠状动脉疾病(CAD)。研究人员利用临床数据和冠状动脉计算机断层血管成像(CCTA)图像来训练深度学习模型。一项研究显示8使用不同的机器学习模型基于临床数据预测心血管疾病(CVD)。研究人员使用的模型包括决策树(DTs)、k近邻(KNN)和随机森林(RFs)。利用这些模型,作者报告了在预测CVD时具有很高的准确率。同样,在一项由的研究中9,机器学习技术被用来确定哪些因素会影响心脏病的风险。作者利用了国家健康和营养检查调查(NHANES)数据来确定与冠心病相关的风险因素。另一项研究10评估了各种机器学习算法在预测心脏病方面的有效性。作者报告称,模型在预测心脏病方面实现了高准确性。
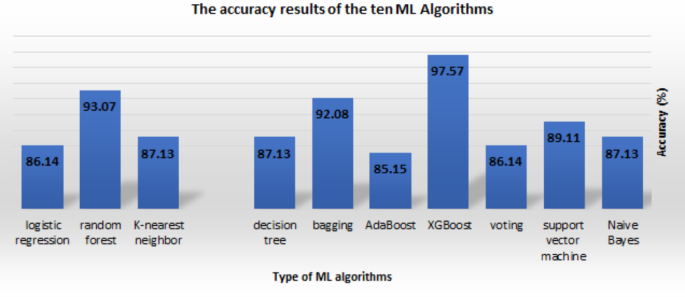
许多研究人员使用机器学习分类技术来预测心脏病。这项工作中使用的机器学习分类器在检测心血管疾病的风险方面显示出有前景的结果。11,12,13,14,15,16,17,18,19,20,21,22,23LR、RF 和 KNN 算法在分类心血管疾病(CVD)风险方面表现出高准确性。集成学习技术,如装袋(bagging)、AdaBoost 和投票(voting),与单一分类器相比提高了分类精度。使用多个机器学习分类器可以提高 CVD 风险预测的准确性。我们可以在此领域进行进一步的研究以改善 CVD 的预测和诊断。机器学习是 HD 预测的强大工具,它有可能通过早期检测和个性化治疗来改善患者预后。这一部分从比较用于预测心脏病的十种机器学习分类器开始。这些分类器包括朴素贝叶斯、SVM、投票法、XGBoost、AdaBoost、装袋法、KNN、DT、RF 和 LR(见表)。1结果表明,机器学习分类器可以提高心脏病预测的准确性,最高达到97%。28使用AdaBoost、决策树(DT)、随机森林(RF)、K近邻(KNN)和逻辑回归(LR)在UCI数据集上进行。一些研究利用了明尼苏达心脏疾病数据集(CHDD),准确率从77%不等32至92%30使用诸如AdaBoost、决策树(DT)、随机森林(RF)、K近邻(KNN)、逻辑回归(LR)、支持向量机(SVM)和朴素贝叶斯等机器学习算法。因此,机器学习分类器可以提高心脏病预测的准确性,从而实现早期检测和个人化治疗。然而,为了验证这些分类器在更大数据集上的准确性,并增加结果的通用性和可重复性,仍需进行更多的研究。
本研究的目的是为心脏病预测提供一种机器学习方法。我们在大型、开放访问的心脏病预测数据集上评估了各种机器学习算法。这项研究旨在构建一种创新的机器学习技术,能够准确分类多个高分辨率的数据集,并对其性能与其他顶级模型进行比较。该研究的一个关键贡献是使用了一个私有的高清数据集。埃及专业医院自愿提供了2022年至2024年间共200个样本的数据,我们从这些参与者中收集了大约13个特征信息。本工作处理的是埃及和沙特阿拉伯对早期心脏衰竭预测的紧迫需求,在这两个国家,心脏衰竭的发生率正在迅速上升。作者通过将机器学习分类算法应用于包含CHDD(冠状动脉疾病数据集)和私有数据集的组合数据集中来评估所提出的模型性能。使用组合数据集,这种方法能够准确地预测心脏衰竭,并且与之前的研究所采用的方法相比是一种新的方法。研究的目标是利用组合数据集以及SF-2特征子集进行心脏衰竭的预测。我们实现了以下指标:精确度为97.57%,灵敏度为96.61%,特异性为90.48%,精准率为95.00%,F1得分为92.68%,AUC值为98%。为了理解系统如何预测其结果,开发了一种可解释的人工智能方法,利用SHAP(Shapley Additive Explanations)技术。本研究中另一个重要方面是使用SMOTE来增加数据集中平衡案例的总数,以提高心脏衰竭预测的表现。所提出的技巧是在使用SMOTE进行数据集均衡化的训练下完成的,以此增强心脏病预测性能。本文应用的所有机器学习方法还通过优化超参数进行了调整。当在组合的数据集和SF-2特征子集上使用时,经过优化超参数后的方法实现了97.57%的准确率。此外,为了识别能获得最精确心脏衰竭预测结果的分类器,本研究评估了10种不同的机器学习分类算法。通过评估十种算法的表现,确定XGBoost技术是一种高度准确的心脏病预测分类器。通过应用领域适应方法展示该应用程序的能力,这表明所提出的这种方法可以在本文使用的初始数据集之外的各种环境和社区中实施。
该研究提议提供了多个独特的贡献,显著提升了其在心脏病预测领域的新颖性和相关性,包括:
-
1.
全面的特征选择方法论我们的研究引入了一种全面的特征选择过程,使用了三种不同的方法:卡方检验、方差分析(ANOVA)和互信息(MI)。与以往的研究可能依赖单一或不够系统的方法不同,我们通过这些方法严格评估了每个特征的重要性,从而产生了三个专门化的特征子集(SF-1、SF-2、SF-3)。这种研究方法确保了预测模型中只包含最相关和最具影响力的特征,从而提高了其准确性和效率。
-
2.
多个机器学习分类器的评估我们对包括XGBoost、AdaBoost等最新算法和集成方法在内的十种不同机器学习分类器进行了广泛的比较分析。通过在各种算法上进行广泛评估并使用选定的特征子集,我们确定了最佳的分类器-特征组合,而这一主题在现有文献中鲜有涉及。我们展示了具有SF-2特征子集的XGBoost分类器的优越性能,强调了我们的特征选择策略的重要性。
-
3.
利用私人健康数据集除了使用公开的数据集之外,我们还采用了一个未在以往研究中探索过的私人健康数据集。这一新颖数据集的加入为我们的研究增添了一层原创性,因为它使我们能够验证模型在不同数据源上的稳健性和泛化能力。该数据集的结果提供了对心脏病预测的新视角,特别是在那些类似数据尚未经过深入分析的领域。
-
4.
我们实施了合成少数类过采样技术(SMOTE)来解决数据不平衡的问题,这在医学数据集中常常是一个挑战。通过确保训练数据的平衡性,我们的研究提高了预测模型的可靠性和准确性,特别是在早期心脏病检测方面。这一步骤对于提高模型在实际应用场景中的实用性至关重要,在这些场景中数据不平衡是很常见的。
-
5.
可解释的人工智能方法的发展据我们所知,将SHAP(Shapley Additive Explanations)方法论整合到心脏疾病预测的可解释人工智能框架中是一项新颖的贡献。这种方法不仅通过提供对预测过程的透明度来增强模型的信任度,还帮助医疗专业人员理解影响诊断的潜在因素。
-
6.
通过手机应用程序的实际应用最后,基于最佳性能的机器学习模型开发移动应用程序标志着向实际应用的重要一步。该应用程序允许用户输入症状并快速获得心脏病预测结果,为早期检测提供了一个用户友好且成本效益高的工具。将我们的研究成果转化为具体的产品突显了我们研究的新颖性,因为它弥合了理论研究与实用医疗解决方案之间的差距。
方法
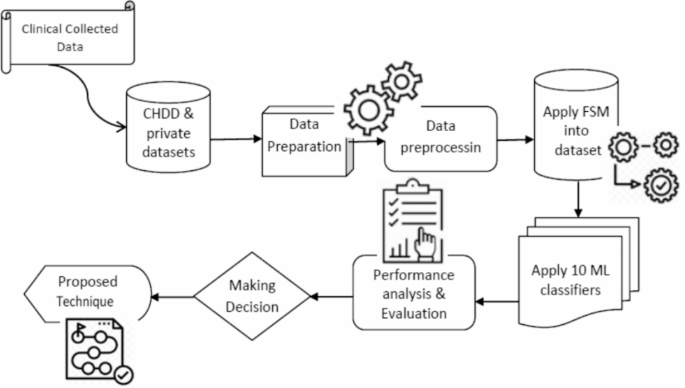
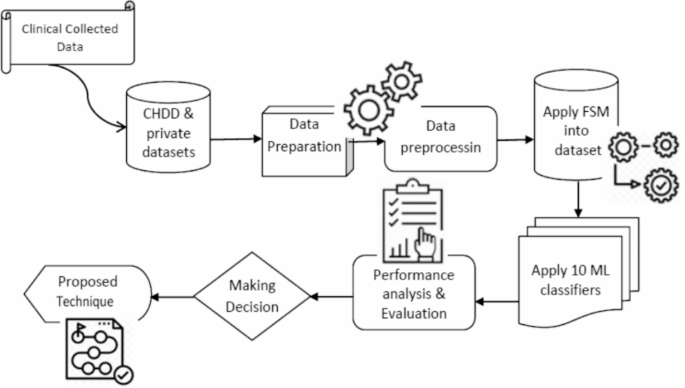
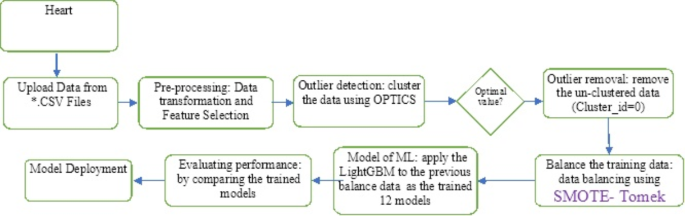
图1展示了所提议系统预测心脏病的序列。我们首先收集并预处理了数据集,以移除任何必要的不一致性,例如用平均值替换空值。我们将数据集分为两个不同的组,分别称为测试数据集和训练数据集。接下来,我们实施了几种不同的分类算法,以确定哪种算法在这两个数据集中实现了最高的准确性。
提出的方法论
本研究调查了诸如朴素贝叶斯、支持向量机(SVM)、投票法、XGBoost、AdaBoost、装袋法(Bagging)、决策树(DT)、K近邻(KNN)、随机森林(RF)和逻辑回归(LR)等机器学习技术。这些算法可以帮助医生和数据分析师正确诊断心脏病。本文结合了最近关于心血管疾病的数据,以及相关的期刊、研究和出版物。方法如下:1提供了建议模型的框架。该方法论是一系列将原始数据转化为可消费和可识别的数据模式的步骤。所提出的方法包括三个阶段:第一阶段是数据收集;第二阶段提取特定特征值;第三阶段是数据分析,如图所示。1根据采用的程序,数据预处理涉及处理缺失值、清洗数据和规范化数据。2我们随后使用十种分类器(A1、A2、……、A10)对预处理的数据进行了分类。最后,在将建议的模型付诸实践后,我们使用一系列性能度量对其性能和准确性进行了评估。该模型开发了一个可靠的心脏病预测系统(RPSHD),并采用了多种分类器。此模型使用了包括年龄、性别、胆固醇水平、血压以及心电图在内的13个医学因素进行预测。3.
数据集和数据集特征
本研究使用了CHDD数据集和一个私有数据集来进行心脏病预测。CHDD数据集包含303个样本,而私有数据集包含200个样本,并且它们具有相同的特征。合并后的数据集共有503条记录,每个记录与13个特征相关联(包括人口统计学、临床和实验室参数)。这些数据集中有许多可用于心脏病预测的特征,包括年龄,性别,血压,胆固醇水平,心电图读数-ECG,胸痛,运动诱发的心绞痛,空腹血糖,达到的最大心率,旧峰值,冠状动脉,地中海贫血,以及其他临床和实验室测量结果如表所示2称为结果变量的“目标”取一个二进制值并指向上述的内容心脏疾病预测特征(即它表示是否存在心脏疾病)。
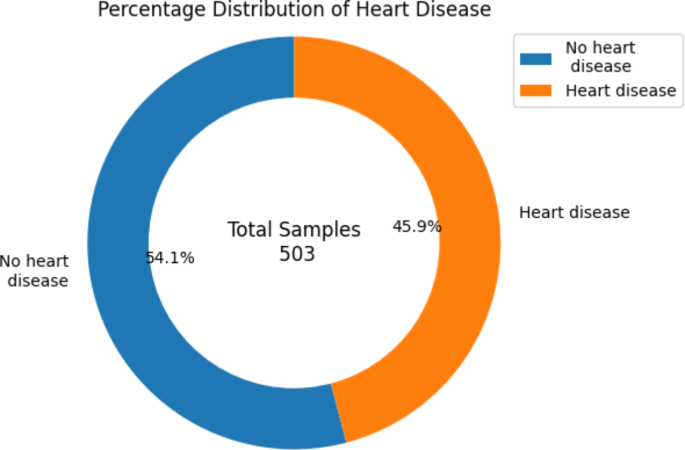
图2展示了合并数据集中患有心脏病个体的百分比分布。总共收集了503个样本,其中45.9%的人被诊断出患有HD,而其余54.1%的个体未感染该疾病。
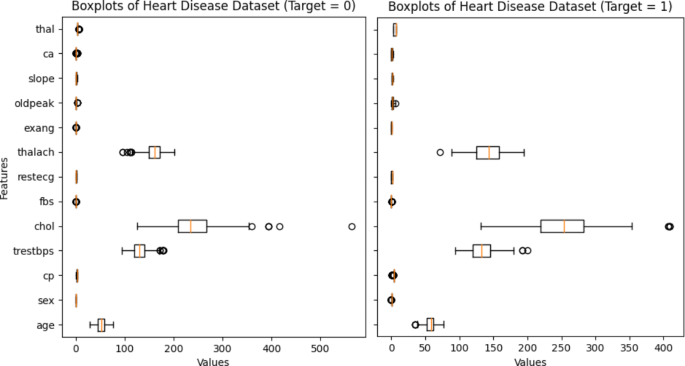
箱线图是一种有效的可视化技术,用于理解数据的分布并识别潜在的离群值。通过将箱线图应用于与HD相关的数据集,可以洞察各种与HD相关特征或变量的分布情况。HD数据集的箱线图如图所示。3箱线图用于展示此图中HD检测得分的分布情况。我们获得的每个图表都存在异常值。去掉这些异常值会导致数据的中位数下降,这可能会使准确检测HD变得更加困难。另一方面,这种方法比其他方法更有益;通过在医疗干预最有效的早期阶段识别心脏病感染,这种诊断可以挽救生命。
数据集准备
在这项研究中,对收集的数据进行了预处理。CHDD中有四个不准确的CMV记录和两个错误的TS条目。错误数据被更新为所有字段的最佳可能值。然后,使用StandardScaler将所有特征归一化到相关的系数,确保每个特征具有零均值和单位方差。通过考虑患者的心脏病史和其他医疗问题,选择了有组织且完整的增强数据集。
本研究中使用的数据集是由可访问的公共WBCD和选定的私人数据集组合而成。以这种方式划分两个数据集使我们能够使用保留验证方法。在本次研究中,25%的数据用于测试数据集,而75%的数据用于训练数据集。在这项研究中,互信息法被用来衡量变量之间的相互依赖性。数值越大表示依赖性和信息收集程度越高。
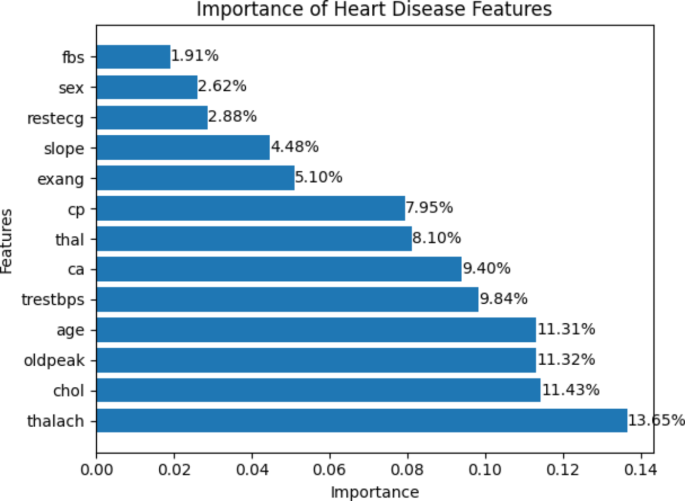
特征的重要性提供了关于数据集中每个特征的相关性和预测能力的宝贵见解。使用这种互惠信息技术,心率峰值(thalach)该特征被赋予最高的值13.65%,而fbs该特征的重要性最低,为1.91%,如图所示。4.
特征选择
在这项研究中,我们使用特征选择和分类方法Scikit-learnPython模块20最初,使用了几种不同的机器学习分类器(包括随机森林、逻辑回归、K近邻、集成、决策树、AdaBoost、XGBoost、支持向量机、投票和朴素贝叶斯)对处理后的数据集进行了分析,并对其整体准确性进行了评估。在第二步中,我们使用了Python的Seaborn库创建相关矩阵的热图和其他不同数据集之间的相关性可视化。第三步是广泛地特征选择方法(有限状态机)如方差分析(ANOVA)、卡方检验和互信息(MI)被应用。这些策略在表中解释。3并分别用缩写FSM1、FSM2和FSM3表示。最后,对识别出的特征比较了几种算法的性能。使用了以下方法证明分析的有效性:准确性, 特异性,精度,敏感度,和F1分数. 的标准缩放器该方法用于在特征传递给算法之前对其标准化。
不同特征选择方法的结果
每个特征对的F值是通过使用方差分析F值技术以及特征权重来确定的。表 (注:原文最后一部分“Table”缺少具体内容,因此保留原样)4(a) 呈现了ANOVA F检验的结果。EIA、CPT和OP特征对分数最为重要,而RES、CM和FBS特征贡献最小。卡方检验是另一种确定每个特征与目标相关程度的方法。表4(b) 显示了卡方检验结果。在此方法中,前三项最重要的特征是MHR、OP和CMV,而TS、REC和FBS分别是相对不重要的特征。FSM3中使用了MI技术,以评估特征之间的相互依赖程度,该方法计算它们之间的互信息。得分为0表示两个特征之间完全独立;数值越大表示依赖性越强。MI得分结果见表4(c). 在这种情况下,CPT、TS和CMV是相互依赖性最强的三个特征,而FBS和REC是互不相关的特征。表4说明了可用于预测患心脏病概率的重要因素。此外,REC、FBS、RBP和CM在所有三个FSMs中的总分数都较低。由于这些特征,根据它们的分数选择了三个不同的组。分别为这三个不同特征集合赋予了SF-1、SF-2和SF-3的缩写。表5显示了这些被选中进行进一步调查的功能集合。
根据研究对性能标准的评估(见表)6),我们选择了使用结合数据集和SF-2特征子集的XGBoost分类器与SMOTE。我们将最准确的技术嵌入到移动应用中,并使用包括Android Studio 14.0、Python 3.10、Spyder、Java 11和Pickle 5在内的多种集成开发环境(IDE)部署模型。26.
使用SMOTE和SHAP方法
为了克服数据集不平衡的问题,机器学习预测应用采用了强大的合成少数类过采样技术(SMOTE)。该技术在各种应用中扮演着重要角色。
-
1.
平衡类别分布在许多预测任务中,例如医学诊断和预测,数据集往往是不平衡的。这意味着某个特定类别(通常是感兴趣的类别)的代表性低于其他类别。SMOTE通过插值少数类样本来创建合成的少数类样本。这种平衡的类别分布确保了预测模型能够从足够的少数类样本中学习。
-
2.
提高预测准确性在预测建模中,不平衡的数据集可能导致模型偏向于多数类,从而导致预测少数类时表现不佳。准确预测少数类是一个重要的挑战。应用SMOTE可以在一个更加平衡的数据集上训练模型,提高准确性和预测性能,特别是在少数类的预测方面。这在错失少数类(例如疾病病例)可能会产生严重后果的应用中至关重要。
-
3.
提高召回率和精确度在不平衡数据集上训练的预测模型通常对多数类具有较高的精度,但对少数类的召回率较低。这意味着它们会错过大量少数类实例,即使它们识别出的实例是准确的。SMOTE有助于提高召回率而不牺牲精度,从而生成更加平衡和有效的模型。实际上,这意味着该模型能够更好地识别所有相关案例,而不仅仅是某些特定案例。
-
4.
减少模型偏见在预测应用中,一个存在偏见的模型可能导致不公平的结果,尤其是在少数类样本不足的情况下。通过在训练过程中让模型接触足够数量的少数类示例,SMOTE(综合过采样技术)可以缓解这种偏差。这有助于创建一个更加公平的模型,在所有类别上都能做出更公正的预测。
-
5.
改进泛化能力在不平衡数据上训练的模型可能在训练期间对多数类表现良好,但它们无法很好地泛化到新的、未见过的数据中,特别是对于少数类。通过使用SMOTE来创建一个平衡的训练集,模型能够更好地将其预测泛化到新数据中,在实际应用中表现出更可靠和一致的性能。
-
6.
增强部署的健壮性在部署的机器学习应用程序中,健壮性是关键。预测模型经常面临偏斜或不平衡的真实世界数据。SMOTE有助于创建一个更健壮的模型,能够更有效地处理此类数据,降低生产环境中的失败风险。这对于像预测维护这样的应用至关重要,在这些应用中,识别罕见但关键的故障可以防止昂贵的停机时间。
另一方面,SHAP(夏普利加性解释)是机器学习中一个强大的工具,有助于解释复杂模型所作出的预测。以下是SHAP在机器学习应用中的优势:
-
1.
增强透明度: SHAP使黑盒模型更加透明,增强了用户和利益相关者的信任。这在金融、医疗和法律等行业尤为重要,因为在这些行业中理解模型决策至关重要。
-
2.
合规性许多行业受到要求模型决策可解释性的法规的约束。SHAP通过为每个决策提供清晰易懂的解释来确保合规性,这便于文档记录并与监管机构分享。
-
3.
提升用户信任和采用率当最终用户了解模型为何做出某些预测时,他们更有可能信任并采用这项技术。用户界面可以融入SHAP解释,以提高人工智能应用程序的用户友好性。
-
4.
可操作的洞察力SHAP 不仅解释预测结果;它还提供可操作的见解。例如,在预测模型中,SHAP 可以识别有效特征的关键因素,使医生能够采取主动措施来检测疾病。
-
5.
促进协作: SHAP解释可以弥合数据科学家和非技术利益相关者之间的差距,促进更好的沟通与协作。通过提供对模型行为的共同理解,团队可以更有效地协同工作。
实验结果与分析
我们使用Jupyter Notebook 7从数据集中预测心脏病。它简化了数据集中不同数据关系图的可视化,并且便于创建包含实时编码的文档。这项研究的第一步是使用Python的Pandas和NumPy库(版本24.2.0)清理CHDD。接下来,标准尺度Python的r方法 注意:这里的"r method"在Python中没有特定含义,可能是上下文缺失或表述不完整。如果指的是原始字符串(raw string),正确的表达是'r'前缀或者're'模块中的某些方法,请提供更多信息以便更准确地翻译和理解。根据要求只输出翻译结果,则按照字面意思翻译为“Python的r方法”。Scikit-learn模块预处理数据集34过程的第二步使用特征选择方法计算每个特征的重要性,生成三组特征(SF)。第三步,我们将数据集划分为训练集和测试集。我们用75%的数据进行训练,剩余25%用于测试。最后,我们使用这75%的训练数据训练了十种不同的机器学习算法,并选择了性能最佳的方法来预测心脏病。35.
绩效评估
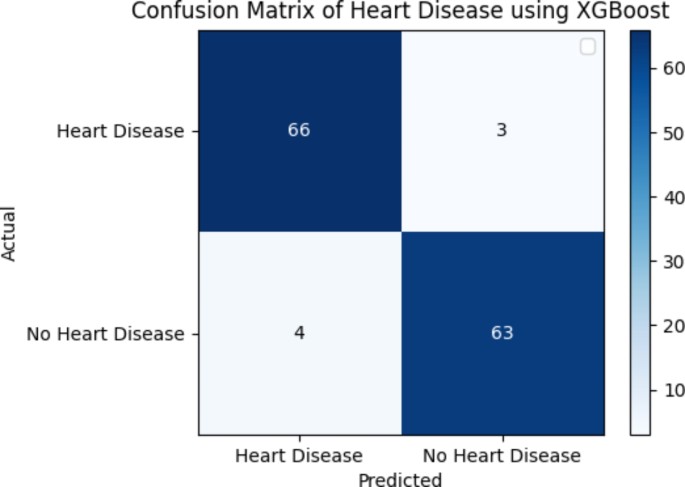
在这一小节中,作者评估并解释了所提议系统的性能。作者使用诸如准确率、灵敏度、特异性和F1值等评价指标展示了各种算法及其比较性能。我们利用真阳性(TP)、真阴性(TN)、假阳性(FP)和假阴性(FN)数据来评估这些性能指标。下一小节将重点介绍这些测量方法。在此次评估之后,我们提供了产生最佳结果的算法。图5说明了混淆矩阵在评估分类模型性能中的应用。
图5展示了T的预测值P, FP, TN,和FN对于使用SMOTE的XGBoost分类器,混淆矩阵中的每个元素代表实际类别和预测类别具有特定标签的案例数量。例如,矩阵中有总计63个病例(真正例TP)被正确分类为心脏病,3个病例(假正例FP)被误诊为“心脏病”,4个病例(假反例FN)被错误地归类为“无心脏病”,以及66个病例(真反例TN)被正确区分为与“心脏病”不同的类别。
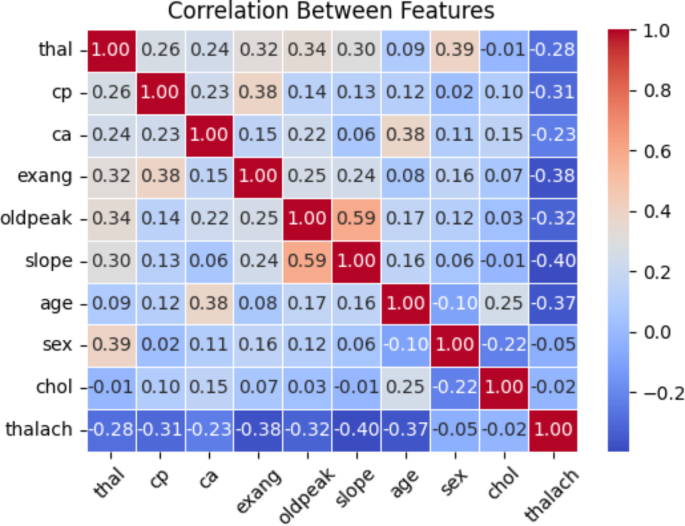
图6展示了使用SMOTE处理后的SF-2重要特征之间的相关性。y轴的值包括thalach、chol、sex、age、slope、exang、oldpeak、ca.、cp.和thal。正或负的相关系数表明了两个变量之间存在显著关系,而−1和1表示没有关联。需要注意的是,唯一可以通过相关性检测到的是变量之间的线性联系。患者的预测结果与这些变量中的每一个至少有70%的相关性。
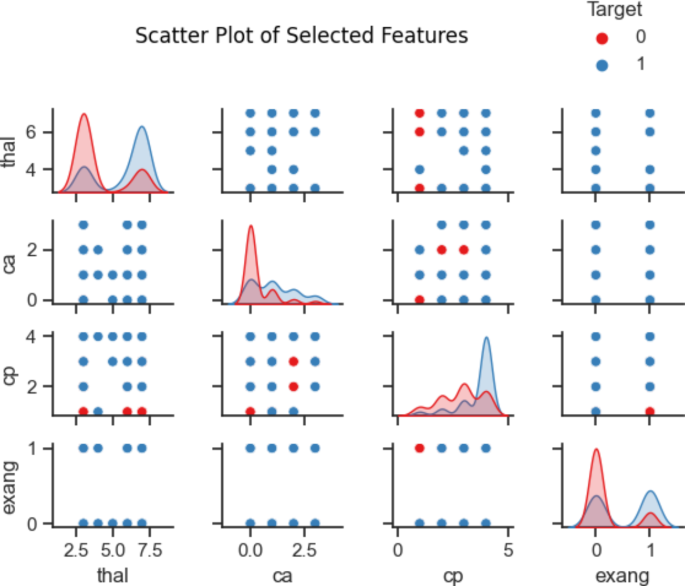
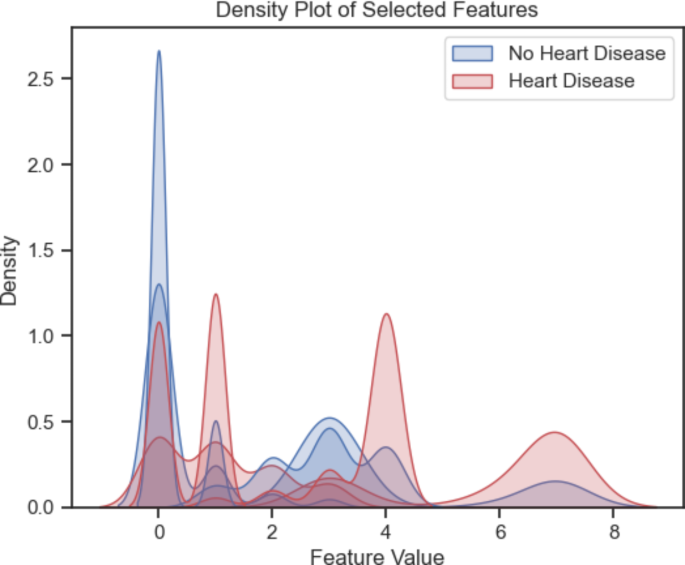
图表7和8显示SF-2数据集中四个选定特征之间的散点图和密度图。这些散点图和密度图有助于探索HD数据集中的变量关系和分布情况。它们可以提供关于这四个变量(exang、cp、ca、thal)之间可能存在的相关性、集中度、异常值和模式的洞察。
-
准确性提出的模型的准确性被开发出来以确定准确分类的样本所占的百分比。准确性是使用给定的公式( Eq. )计算的。1),这是基于混淆矩阵的:
$$\text{准确率}=\frac{{\text{T}}_{\text{P}}+{\text{T}}_{\text{N}}}{{\text{T}}_{\text{P}}+{\text{T}}_{\text{N}}+{\text{F}}_{\text{P}}+{\text{F}}_{\text{N}}}$$
(1)
-
敏感度(或者)回忆): 感敏度衡量真正阳性结果的比率,并暗示所有值都应被正向评估。此外,感敏度计算为“正确检测到的阳性样本的比例”。感敏度通过以下公式确定:
$$\:\text{灵敏度}=\frac{{\text{T}}_{\text{P}}}{{\text{T}}_{\text{P}}+{\text{F}}_{\text{N}}}$$
(2)
-
特异性它预测所有值都将为负,并通过计算真实负情况的比例来确定。特异性是通过数学方法确定的。
$$\text{特异度}=1-\left(\frac{\text{FP}}{\text{FP}+\text{TN}}\right)$$
(3)
-
精度它确定分类器的准确性,并可从给定的信息中计算得出。这通过比较实际真正例(TP)与预测真正例(TP)来呈现。(公式 Eq.)4准确性度量如何验证所提出方法的行为:
$$\text{精确度}=\frac{{\text{T}}_{\text{P}}}{{\text{T}}_{\text{P}}+{\text{F}}_{\text{P}}}$$
(4)
-
F值这是一个用于评估分类模型效果的统计度量。它通过计算准确率和召回率的调和平均值来实现,给这两个指标赋予相等的权重。这使得可以使用一个综合考虑了召回率和精确率的单一评分来描述并比较模型的表现,并且该分数是通过以下公式计算得出的:
$$\text{F}-\text{值}=\frac{2*\left(\text{精确度*召回率}\right)}{\text{精确度+召回率}}$$
(5)
分类器的性能已使用混淆矩阵表示和评估,如图所示。5. T (由于提供的文本极其简短且缺乏具体意义,“T”没有明确的上下文,因此直接输出原文。如果有特定背景或要求,请提供更详细的信息以便准确翻译。)注意:根据指示“如果没有实际内容需要翻译,则输出原文,不要添加任何注释”,这里仅呈现了原始符号“T”。P衡量被准确分类到患病阳性类的个体数量。健康人群被适当标记为阴性类的比例被称为特异性(TN)。将健康人错误诊断为生病的次数称为误诊率(F,这里的表述可能是指假阳性率FP,但原文不完全明确)。为了更精准,请确认具体术语需求。若直接翻译: 衡量被准确分类到患病阳性类的个体数量。健康人群被适当标记为阴性类的比例被称为TN。将健康人错误诊断为生病的次数称为F。P当健康人数被误判时,这被称为F类错误N表中展示了10种机器学习算法之间各种性能指标的比较。6这些AI分类器被应用于包含SF-1、SF-2和SF-3特征子集的组合数据集中。基于其在SF-2特征组中的准确率97.75%,灵敏度96.61%,特异度90.48%,精确率95.00%以及F1分数92.68%(见表)6),XGBoost分类器表现最佳。
系统性能的实验评估
表格6展示了每种技术的准确性以及使用这些算法进行分析后的处理数据集。就每种技术的准确度而言,A4 对 SF-2 的精度计算最准确(97.57%),其次是它对 SF-1 和 SF-3 的精度计算(分别为 93.17% 和 94.19%)。A9 计算出所有三个 SF 的整体精度为 93.07%,位居第二。另一方面,A5 确定在所有分类器中,SF-1 和 SF-3 的准确度较低(85.15%)。同样地,A3 和 A10 分别提供了针对 SF-2 和 SF-3 较低的精度水平(分别为 86.14% 和 86.12%)。其他方法的准确性在 87.13% 到 90.00% 之间。此外,这一发现表明使用 SF-2 的 XGBoost 算法方法对处理数据集最有效。图9展示了使用SF-2的十种机器学习技术可能达到的准确率范围。
本研究评估了所有算法的灵敏度。表 6显示了使用SF-1、SF-2和SF-3分别从十种机器学习技术中获得的敏感性得分。A5对SF-3的敏感度最低(88.14%)。A8对SF-1和SF-3的评分分别为89.83%和89.83%。A4(XGBoost)报告了SF-2最高的敏感度,为96.61%;A2、A3、A4、A6和A9报告了第二高的敏感度,为94.92%。
我们对这些技术中的每一种都进行了特异性分析,见表。6总结了结果。A3在SF-2和FS-3中的得分最低(73.81%)。根据分析,A4和A9在所有SFs中的得分最高(90.48%)。与其它技术的结果相比,A7仅在SF-3中(92.86%)提供了最佳分数。
我们采取了若干策略来降低过拟合的风险,并确保提出的心脏病预测模型在现实世界中的适用性,包括(1)交叉验证我们使用了Python(利用scikit-learn)中的k折交叉验证技术来评估模型在数据多个子集上的泛化性能。这有助于识别不易过拟合的模型,并提供其真实性能更可靠的估计。(2)正则化:引入正则化技术,如L1或L2正则化、 dropout 或提前停止,以防止模型变得过于复杂并降低过拟合的风险。(3) 特征工程:除了使用ANOVA、卡方检验和MI等特征选择方法外,我们还扩展了工作范围,包括能够捕捉有意义的关系和与心脏病预测相关的领域知识的特征工程技术。(4)外部验证在独立的数据集或真实世界的患者数据上验证模型,以评估它们在各种环境中的性能,并确保其在临床实践中的可靠性。
讨论
本研究使用了一个结合数据集(CHDD和私人数据集)进行测试和训练,实施了多种机器学习技术以实现对心血管疾病的早期识别。然后,我们采用领域适应方法在源数据集和目标数据集上测试并训练了该机器学习模型。首先,我们在包含200个案例的私人数据集上训练了本研究中提出的HD预测技术。之后,我们使用一个包括503个案例的综合数据集对系统进行了评估。具体来说,我们总共采用了十个著名的机器学习算法,包括朴素贝叶斯、支持向量机(SVM)、投票法、XGBoost、AdaBoost、袋装法、决策树(DT)、K近邻(KNN)、随机森林(RF)和逻辑回归(LR),分别表示为(A1, A2,…,A10),如表所示。6,每个都具有独特的选定特征集。ANOVA F统计量、卡方检验和MI统计量是用于分组更能预测心血管疾病(CVD)的重要因素的统计方法。我们使用了五种不同的评估标准:准确率、敏感性、精确度、特异性和F1分数来比较和评价使用SMOTE的不同机器学习技术的表现。实验表明,对于SF-2,算法A4具有最高的准确率(97.57%)。对于表中所示的所有三个SF,算法A9具有第二高的准确率(93.17%)。6A4 同样在检测 SF-2 时获得了最高的灵敏度得分(96.61%)和最佳的特异度得分(90.48%),如表所示。6F1分数的结果表明,A4在SF-2中的得分最高,为92.68%(见表)6),而A9在SF-1、SF-2和SF-3上获得了最高的分数91.57%,A6则在SF-2上获得了最高的分数90.24%。由于A4与SF-2结合使用时表现最佳,因此该方法在准确性、特异性和敏感性方面是最可靠的。就F1得分而言,A9是所有SF中更准确的预测模型,使其成为总体第二好的预测算法。根据这项研究,我们得出结论认为它提供了最高的性能指标。因此,我们可以得出结论,XGBoost是一种有效的预测心脏病的方法。在结合多个不同的机器学习算法的结果时,大多数情况下的准确性范围为85.15%至97.57%。
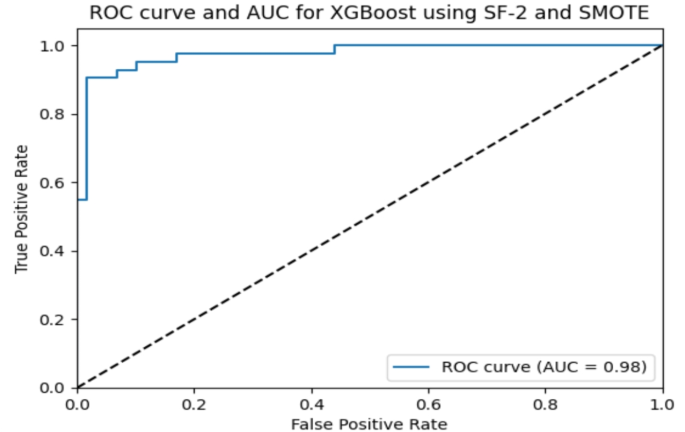
XGBoost分类器与SF-2的接收者操作特征(ROC)曲线如图所示。10该曲线显示了模型在所有分类阈值上的表现情况,AUC为0.98(见表)7).
一种应用SHAP库的可解释的人工智能方法用于理解模型的决策过程。
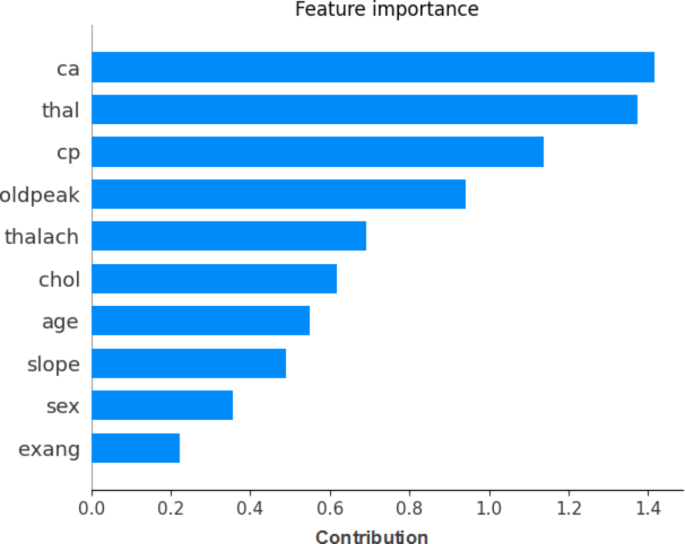
图11展示了SHAP库、XGBoost以及SMOTE特征的重要性。
使用机器学习分类器进行HD预测是本工作的目标。实验结果证明,XGBoost算法在预测HD发生的准确性方面最高。根据基于互信息的特征选择方法,以下特征被归类为对HD预测重要的特征:thalach、chol、oldpeak、age、trestbps、ca.、thal、cp.、exang、slope、restecg、sex和fbs。我们使用了SMOTE方法来优化超参数,并通过收集到的数据进行过采样处理。结合使用XGBoost技术和SMOTE产生了最佳结果。本研究达到了使用组合数据集预测HD的目标,实验结果显示准确率为97.57%,灵敏度为96.61%,特异度为90.48%,精确度为95.00%,F1得分为92.68%,AUC值为98%。
在心脏病预测的背景下,高达97.57%的高准确率表明XGBoost模型非常可靠地区分了患有和未患心脏病的患者。然而,重要的是要解释这一高准确性在临床实践中的意义:
-
1.
早期检测该模型的高灵敏度(96.61%)表明它能够有效识别心脏病早期阶段的患者,这对于及时干预和治疗至关重要。
-
2.
减少假阳性:特异性(90.48%)表明假阳性的率相对较低,意味着较少的患者会被误诊为心脏病,从而减少不必要的焦虑和治疗。
-
3.
平衡预测高的F1分数(92.68%)反映了精确度(在存在心脏病时正确预测)和召回率(尽可能识别真正病例)之间的平衡,这对于误报和漏报都会产生严重后果的实际应用至关重要。
要理解这一突破,必须将XGBoost的性能与现有的心脏病预测黄金标准进行比较,这些标准通常包括已经确立的临床评分系统或其他在医疗保健领域广泛接受的机器学习模型。
-
1.
如果XGBoost超越现有模型这一准确率提升至97.57%将标志着一个显著的进步,可能为临床医生提供一个更为可靠的工具。
-
2.
如果与现行标准相比如果这种准确性仅略好或与当前方法相当,必须对改进的意义进行批判性评估。模型的泛化能力、融入临床工作流程的简便性以及对于医疗专业人员的可解释性成为决定其是否真正代表突破的关键因素。
要将此性能视为一项突破,未来的工作必须包含以下理由:
-
与基线方法的比较证明XGBoost在准确率和其他关键指标上显著优于现有的预测方法。
-
临床影响讨论这一改进如何能够转化为更好的患者预后,例如通过更准确的早期诊断来减少死亡率或发病率。
-
可扩展性和实现描述该模型与当前医疗系统的潜在整合及其在真实世界环境中对各种患者群体的适用性。
提出的基于机器学习的心脏疾病预测技术有可能改善医疗保健。通过允许早期检测和治疗,准确地预测心脏疾病可以大大降低死亡率。在专家资源有限的情况下,医生可以使用此工具来诊断患者。将该技术与电子健康记录(EHR)系统集成,可以实现实时风险评估,从而改善患者的预后和决策制定。
这项研究的移动应用程序可能有助于患者,特别是那些身处偏远地区或无法获得医疗保健的人自我评估。它允许用户输入他们的症状并获取快速的心脏疾病风险评估,促使他们寻求医疗帮助。这一工具使个人能够掌握自己的健康状况,这可能会帮助更早地诊断和治疗心脏问题。
该研究通过提供一种可扩展且成本效益高的心脏疾病预测解决方案,为数字健康改进的更广泛目标做出了贡献。作者利用机器学习和可解释的人工智能(通过SHAP方法),创建了一个不仅准确而且可解释的系统,确保医疗专业人员能够信任并理解模型所做出的预测。这种透明度对于在临床实践中采用人工智能工具至关重要。
此外,移动应用程序的使用扩展了这项技术的覆盖范围,使其能够服务于更广泛的人群。这种医疗工具的普及化与全球改善公共卫生和减少心血管疾病负担的努力相吻合,而心血管疾病是全球死亡的主要原因。
限制事项
尽管基于机器学习的心脏病预测技术具有令人鼓舞的结果和潜在用途,但仍需考虑几个限制因素:
-
1.
数据集的质量和可用性机器学习模型的性能和可靠性取决于测试和训练数据集的质量和可用性。我们在研究中使用了克利夫兰心脏疾病数据以及私人数据库。可能存在可用性、代表性及数据质量方面的限制。这种限制可能会使得将提出的方法应用于更多样化来源的更广泛样本中变得困难。
-
2.
类别不平衡:SMOTE 生成合成的少数类样本以克服类别不平衡问题,但其有效性取决于数据集和具体情况。在心脏病预测中,当疾病频率可能很低时,类别不平衡成为一个主要问题。类别不平衡会导致模型对多数类表现良好,而对少数类表现不佳,而后者通常是感兴趣的类别。为了解决这个问题,有必要讨论并比较不同的处理类别不平衡的方法作为 SMOTE 的替代方案,例如:
-
类权重优点包括:(a) 实现简单,因为它涉及调整不同类别的错分类惩罚;(b) 不需要修改数据集或生成合成样本,因此计算效率高;以及(c) 在不增加额外复杂性的情况下有效提高模型在少数类上的性能。缺点包括:(a) 假设错分类成本是已知且适当指定的,这在实际中可能并非总是如此;(b) 假设类别之间的决策边界是非线性的或复杂的。
-
集成方法优点包括:(a) 通过汇总由训练在数据平衡子集上的多个基础模型的预测自然地处理类别不平衡;(b) 倾向于对噪声和过拟合具有鲁棒性,使其适合不均衡的数据集;以及(c) 捕获特征与目标变量之间的复杂关系,提高预测性能。缺点包括:(a) 与更简单的算法相比需要更多的计算资源和更长的训练时间;(b) 在最终预测中无法提供对类别的平衡的明确控制。
-
成本敏感学习优势包括:(a) 明确考虑不同类别错误分类的成本,允许对模型行为进行微调;(b) 能够适应不同程度的类别不平衡并相应地调整决策边界。局限性包括:(a) 需要知道错误分类成本,这在实际情况中可能难以收集或具有主观性;(b) 通过调节更多超参数使模型选择变得更加复杂。
-
异常检测优点包括(a)可以在少数类代表罕见或不寻常事件的情况下使用,例如发现罕见的心脏病;以及(b)不需要明确标注少数类实例,这意味着它既可以用于半监督设置也可以用于无监督设置。缺点包括(a)假设少数类实例是异常值或与多数类显著不同,这在实际情况中可能并不总是成立;以及(b)难以检测数据中的细微或复杂模式,尤其是在正常和异常实例之间的界限模糊时。
-
3.
算法选择为了确定预测HD的最佳算法,研究人员使用了多种机器学习技术。然而,所选择的算法是任意的,并可能影响结果。本研究未考虑的其他算法可能会实现不同的权衡或更高的准确性。因此,未来的研究应仔细考虑和评估选定的机器学习算法。
-
4.
领域适应领域适应技术的使用展示了所提出系统的适应性。将该提议的技术应用于各种不同的群体或环境可能仍然会面临一些限制。需要更多的研究来确定该技术在具有不同生活方式、人口统计特征和医疗保健体系的各种人群中的有效性。还必须充分解决与领域适应相关的任何潜在限制和困难。
-
5.
缺失数据该研究并未说明机器学习模型的训练和测试数据集是否包含缺失数据。在现实世界的医疗保健中,缺失数据普遍存在,并且会对预测模型产生严重影响。讨论应集中在如何解决缺失数据导致的错误预测、误诊或治疗延误问题上。作者可以探讨填补缺失值的方法或者针对部分数据集的稳健算法。我们必须处理缺失数据以确保临床预测模型的可靠性和泛化能力。
结论与未来工作
在这项研究中,我们采用多种方法选择特征,并应用了十种不同的机器学习技术结合SMOTE到这些选定的特征上。这一过程使我们能够识别出在预测心脏病方面最有效的关键特征。每个算法根据不同的特征组合产生一个独特的评分。我们使用三种方法来选择特征:ANOVA、卡方检验和MI。我们将这三种方法分别应用于三个选定的特征组,即SF-1、SF-2和SF-3。十个机器学习分类器确定了最佳模型和特征子集。所使用的分类器包括朴素贝叶斯、支持向量机(SVM)、投票算法、XGBoost、AdaBoost、袋式集成(Bagging)、决策树(DT)、K近邻(KNN)、随机森林(RF)和逻辑回归(LR)。我们使用了一个著名的开放访问数据集,并进行了多个交叉验证过程来评估选定的算法并衡量心脏病检测系统的性能准确性。与所有其他算法相比,XGBoost的表现更为显著。XGBoost分类器在SF-2特征子集中表现最佳,准确率达到97.64%,灵敏度为96.61%,特异性为90.48%,精确度为95.00%,F1得分为92.68%,AUC值达到98%。我们使用SHAP技术开发了一种可解释的人工智能方法,以了解系统如何预测其结果。此外,该研究还展示了所提出的系统可以通过领域适应的方法进行调整。本工作通过引入独特的见解和技巧,在基于机器学习的心脏病预测应用程序的领域做出了重要贡献。这些发现有可能帮助埃及和沙特阿拉伯进行心脏病的诊断和预测。
最后,作者们正在开发一款智能手机应用程序,允许用户输入症状并快速准确地预测心脏病。我们将把最佳的XGBoost技术嵌入到移动应用中以预测心脏病,并即时显示检测结果。由于该移动应用是基于症状的心脏病预测工具,在其实施过程中我们会考虑和解决“暗数据”的影响问题。“暗数据”是指因为数据采集限制、报告不善或忽视而存在的未收集或利用的信息。在预测心脏病时,未报告的心脏病案例被视为“黑数据”。因此,在我们未来的工作中,我们将研究暗数据如何影响所提议移动应用程序的现实世界实施,特别是关注以下方面:(1)无症状病例:早期心脏疾病的患者可能不会表现出任何症状。(2)基于症状预测的局限性:模型仅考虑了一组有限的症状。由于诊断测试和影像学检查,心脏病可能会以除典型症状之外的方式表现出来,因此只专注于症状可能会忽略关键迹象。(3)数据收集:缺乏无症状病例可能会对应用程序预测模型的数据集质量产生影响。如果大多数训练数据是有症状的,则模型的预测可能更侧重于有症状的表现形式,从而加剧暗数据的影响。
为了应对黑暗数据效应带来的限制并增强针对心脏病预测的移动应用程序在实际世界中的适用性,我们将考虑若干策略,包括(1)全面风险评估:将预测模型的范围扩大到除症状之外的额外风险因素,如人口统计信息、医疗历史、生活方式因素和生物标志物。(2)与诊断工具集成:连接移动应用与能够测量与心脏健康相关的生理参数(例如血压、心率变异性或心电图(ECG)信号)的诊断设备或可穿戴设备。(3)人群筛查项目:与医疗服务提供者或公共卫生机构合作,推广旨在识别未被诊断的心脏病患者的人群筛查项目。(4)教育和意识提升活动:发起教育计划以提高人们对定期进行心血管检查(即使没有症状)重要性的认识。作者还将为心脏病预测应用程序考虑成本效益论证,提供证据,并考虑包括开发、实施和维护费用在内的各种因素。声称某些功能更便宜需要进行全面评估并与替代方法进行比较,以确保该声明的有效性。
由于无法解释决策过程,基于机器学习的系统开发者倾向于将基于人工智能的应用视为神秘之物。在这项研究中,我们使用了SHAP和特征重要性技术来解释和解读对决策影响最大的显著特征。在我们的未来工作中,计划通过纳入其他可解释的人工智能(XAI)技术来扩展我们的研究,以提高透明度和可解释性,例如:(1)部分依赖图(PDPs):PDPs展示了某个特征与其预期结果之间的联系,同时忽略其他特征。通过分别展示每个特征,我们可以明确了解其对心脏病预测的影响。(2)个体条件期望(Ice)图表: 冰图展示了特征如何影响每个数据点,而不仅仅是平均值。可以更好地理解特征变化对不同人群的影响。(3)局部可解释的模型无关解释(LIME):为了解释预测,LIME在特定样本周围开发局部替代模型。通过改变输入数据并观察预测的变化,LIME接近模型的局部行为,并为具体的预测提供简单的解释。(4)基于规则的模型(如决策树或规则列表)将输入特征直接连接到预测。这些模型解释了诊断心脏病的标准,提供了透明度。通过使用可解释的人工智能方法,用于预测心脏病的机器学习系统可以向医疗保健专业人员和患者提供透明、可解释且具有操作性的见解,促进知情决策并提高对人工智能驱动的医疗应用的信任。
数据可用性
通讯作者将在合理请求的情况下分享研究数据集。
参考文献
世界卫生组织。心血管疾病(CVDs)。在线可得:(2023年)https://www.afro.who.int/健康主题/心血管疾病(访问日期:2023年5月5日)
alom, z. 等人。利用机器学习技术早期检测心力衰竭。载于国际大数据、物联网与机器学习会议论文集,孟加拉国科克斯巴扎尔,2021年9月23日至25日。
戈尔,S.,潘瓦尔,P.,德维迪,D. 和马利,C. 心脏病发作预测的机器学习方法。在智能可持续系统(Nagar A. K., Jat D. S., Marín-Raventós G. & Mishra D. K. 主编) 741–747 ( Springer, 新加坡, 2022).https://doi.org/10.1007/978-981-16-6309-3_70.
古普塔,C.,萨哈,A.,雷迪,N. S.及阿查里亚,U. D. 使用监督机器学习技术进行心脏疾病预测。在物理期刊:大会系列IOP出版社:英国布里斯托尔,卷号2161,页码 012013 (2022).
Shameer, K. 等人。利用电子健康记录数据在多民族人群中预测心血管疾病风险。国际医学信息学杂志. 146, 104335 (2021).
刘等人。基于深度学习的冠状动脉CT造影疾病预测。日本放射线杂志 38 (4), 366–374 (2020).
扎克里亚,N.,拉扎,A.,利亚库特,F.及卡瓦贾,S. G. 基于机器学习的心血管疾病预测分析。医学系统杂志 41 (12), 207 (2017).
杨明,王小,李芳 & 吴军. 使用机器学习方法识别冠心病风险因素:大数据分析。计算机方法与生物医学编程 127, 262–270 (2016).
Ngufor, C., Hossain, A., Ali, S. & Alqudah, A. 心脏病预测的机器学习算法:综述。国际计算机科学与信息安全管理期刊 14 (2), 7–29 (2016).
舒卡特,A.,阿尔沙德,S.,阿里,N.及穆尔塔扎,G. 利用机器学习预测心血管疾病:系统综述。医学系统杂志 44 (8), 162. https://doi.org/10.1007/s10916-020-01563-1 (2020).
Shankar, G. R., Chandrasekaran, K. 和 Babu, K. S. 关于机器学习在心血管疾病预测中潜在应用的分析。医学系统杂志 43 (12), 345. https://doi.org/10.1007/s10916-019-1524-8 (2019).
Khanda达什, N., 阿巴布内赫, E. & 哈尔库达哈, M. 使用机器学习技术预测女性冠心病风险。医学系统杂志 45, 62. https://doi.org/10.1007/s10916-021-01722-6 (2021).
Moon, S., 李, W. 和 Hwang, J. 将机器学习应用于预测心血管疾病。医疗卫生信息学研究 25 (2), 79–86. https://doi.org/10.4258/hir.2019.25.2.79 (2019).
拉克什米,M. & 艾耶莎马里亚姆,A. 用于预测心血管风险的机器学习技术。国际先进科学技术杂志 30 (3), 11913–11921. https://doi.org/10.4399/97888255827001 (2021).
Md, R. 等人. 早期检测心血管自主神经病变:基于特征选择和深度学习特征融合的多类分类模型. 信息融合, 卷 77, 第 70-80 页, 一月 (2022).
王科拉普,A.,瓦迪洛,M. A. & 卡尔辛,V. 心血管疾病早期检测的机器学习分类器。生物医学信息学杂志 88, 44–51. https://doi.org/10.1016/j.jbi.2018.09.003 (2018).
德拉瓦尔,M. R.,莫特瓦尼,M. & 沙拉法扎德赫,M. A. 心血管疾病诊断中特征选择和分类方法的比较研究。医学系统杂志 39 (9), 98. https://doi.org/10.1007/s10916-015-0333-5 (2015).
永勇,金圣,朴盛俊,金智爱。用于第二型糖尿病患者心血管疾病风险预测的决策树临床决策支持系统。计算生物学与医学 89, 413–421. https://doi.org/10.1016/j.compbiomed.2017.08.024 (2017).
米尔扎 Q. Z., 西迪奇 F. A. & 娜格维 S. R. 利用决策树算法预测心脏事件的风险。巴基斯坦医学科学杂志 36 (2), 85–89. https://doi.org/10.12669/pjms.36.2.1511 (2020).
法拉格,A.,法拉格,A.及萨拉姆,A. 使用提升和装袋技术改进心脏病预测。国际创新计算趋势会议(ITCE) proceedings. 90-96https://doi.org/10.1109/ITCE.2016.7473338 (2016).
贾贾里亚,S. & 库马尔,R. 使用集成学习方法预测心血管疾病的风险。软计算 24 (7), 4691–4705. https://doi.org/10.1007/s00500-019-04268-8 (2020).
萨马迪尼,N.,莫加达姆,E.,穆塔梅德,C.及A. M.,基于支持向量机的心血管疾病分类:特征选择与高维数据集视角。医学系统杂志 40 (11), 244. https://doi.org/10.1007/s10916-016-0573-7 (2016).
张旭,张悦,杜欣,李博。XGBoost算法在冠心病临床预测中的应用。中国医学仪器杂志 43 (1), 12–15 (2019).
刘, Y., 李, X. & 任, J. 心脏病预测的机器学习算法比较分析。计算机方法与生物医学编程 200, 105965 (2021).
Hussein, N. S., Mustapha, A. & Othman, Z. A. 心脏病诊断的机器学习技术比较研究。计算机科学与信息系统 17 (4), 773–785 (2020).
阿克巴尔,S.,塔里克,R. & 巴沙拉特,A. 利用不同机器学习方法进行心脏病预测:批判性回顾。环境智能人性化计算 11 (5), 1973–1984 (2020).
扎尔舍纳斯,A.,甘巴扎德,M. & 霍斯拉维,A. 关于用于预测心脏病的机器学习算法比较研究。人工智能医学 98, 44–54 (2019).
考尔,I. & 辛格,G. 关于心脏病预测的机器学习算法比较分析。生物医学信息学杂志 95, 103208 (2019).
李,Y., 贾,W. & 李,J. 比较不同机器学习方法预测心脏病:一个远程医疗案例研究。健康信息与系统科学杂志 6, 7 (2018).
张,X., 周,Y. & 谢,D. 使用机器学习和专家系统技术进行心脏病诊断:综述论文。医学系统杂志 42 (7), 129 (2018).
吴,J. & Roy, J. Stewart, & W. F. 关于心脏病预测的机器学习方法比较研究。《健康护理工程杂志》,7947461 (2017). (2017).
Ahmed, Z., Mohamed, K. & Zeeshan, S. 心脏病风险预测的机器学习算法比较:系统评价。《医疗卫生工程杂志》,7058278 (2016). (2016).
陈X., 胡Z. & 曹Y. 使用决策树和朴素贝叶斯分类器进行心脏病诊断。世界医学物理与生物医学工程大会 14, 1668–1671 (2007).
佩德雷戈萨,F. 等。Scikit-learn:Python中的机器学习。机器学习研究杂志(JMLR) 12, 2825–2830 (2011).
Hosam El-Sofany,S. A.,El-Seoud,O. H.,Karam,Yasser,M.,Abd El-Latif,Islam,A. T. F.及Taj-Eddin 提出的一种使用机器学习通过移动应用预测糖尿病的技术。国际智能系统杂志,卷ID6688934, (2024). https://doi.org/10.1155/2024/6688934, (2024).
Chintan, M. B., Parth, P., Tarang, G. & Pier, L. M.利用机器学习技术算法有效预测心脏病, 16, 88, https://doi.org/10.3390/a16020088, (2023).
致谢
作者感谢卡利德国王大学科研与研究生院通过编号为(RGP1/129/45)的小型团队研究资助此项目。
伦理声明
利益冲突
作者声明没有利益冲突。
伦理批准
本研究未涉及人类参与者、人体组织或任何个人数据。用于此研究的数据集是公开且匿名的,无需伦理审批或知情同意。
附加信息
出版者注释
施普林格·自然对于发表的地图中管辖范围的声明和机构隶属关系保持中立。
权利和许可
开放存取本文采用知识共享署名-非商业性使用-禁止演绎 4.0 国际许可协议进行许可。根据该许可协议,您可以自由地分享、复制和传播本文的任何版本或格式,但必须满足以下条件:(1)为原始作者及来源提供适当的署名;(2)提供指向知识共享许可协议的链接;(3)标明是否修改了授权材料。未经本许可协议的允许,您无权分发根据本文改编的作品或其部分内容。除非另有声明,在此文章中的图片或其他第三方材料均受该文章的知识共享许可协议约束。如果某些内容未包含在文章的知识共享许可协议中,并且您的预期用途超出了法律规定或超出许可范围,则需要直接从版权所有者处获得授权。要查看本许可证的副本,请访问http://creativecommons.org/licenses/by-nc-nd/4.0/.
关于这篇文章
引用这篇文章
埃尔索法尼,H.,布奥莱格,B.及埃尔拉提夫,Y.M.A. 使用机器学习算法和可解释的人工智能方法预测心脏病的技术提案。 Sci Rep 14, 23277 (2024). https://doi.org/10.1038/s41598-024-74656-2
收到:
接受受理:
发布:
DOI: https://doi.org/10.1038/s41598-024-74656-2