The 2024年诺贝尔化学奖被识别的德米斯·哈萨比斯, 约翰·贾姆珀以及大卫·贝克ер利用机器学习来应对生物学上最大的挑战之一:预测蛋白质结构蛋白质的三维结构从头开始设计它们。
今年的奖项因其表彰了一家科技公司所进行的研究而引人注目:DeepMind,这家人工智能研究初创公司在被收购之前开展了这项研究。谷歌在2014年此前大多数的化学诺贝尔奖都授予了学术界的研究人员。许多获奖者随后成立了初创公司,进一步拓展和商业化他们的开创性工作——例如,CRISPR基因编辑技术以及量子点但是,从开始到结束,这项研究并没有在商业领域进行。
尽管物理学和化学的诺贝尔奖分别颁发,但在2024年这两个领域的获奖研究之间有一个迷人的联系。物理学奖��奖成果与化学奖获奖成果之间存在这一有趣的关联。去了两位计算机科学家那里谁奠定了机器学习的基础而化学奖得主因利用机器学习来攻克生物学上最大的谜题之一——蛋白质折叠问题而获奖。
2024年诺贝尔奖强调了这种人工智能的重要性,并展示了今天的科学往往跨越传统界限,融合不同领域以取得突破性成果。
蛋白质折叠的挑战
蛋白质是生命的分子机器。它们构成了我们身体的很大一部分,包括肌肉、酶、激素、血液、头发和软骨。
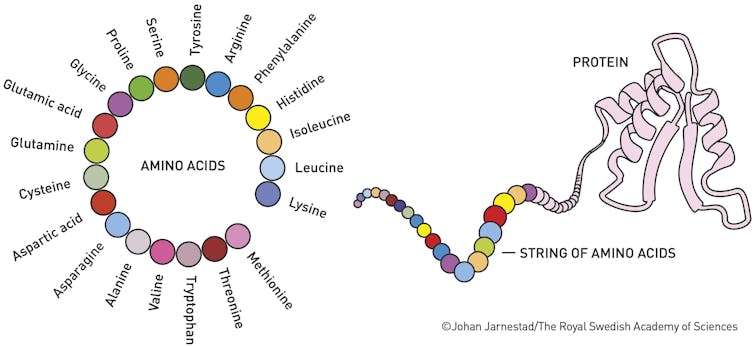
理解蛋白质的结构是很重要的,因为它们的形状决定了其功能。早在1972年,克里斯蒂安·安芬森获得了诺贝尔奖在化学中用于展示蛋白质氨基酸组成单元的序列决定蛋白质的形状这反过来会影响其功能。如果蛋白质错误折叠,它可能无法正常工作,并可能导致诸如疾病之类的病症。阿尔茨海默病, 囊性纤维化或者糖尿病.
一个蛋白质的整体形状取决于组成它的氨基酸中所有原子之间的微小相互作用,包括吸引和排斥。有些原子想在一起,有些则不想。基于数千个这样的化学相互作用,蛋白质会扭曲并折叠成最终的形状。
几十年来,生物学面临的最大挑战之一是仅根据氨基酸序列预测蛋白质的形状。虽然研究人员现在可以预测蛋白质的形状,但我们仍然不清楚蛋白质是如何在几微秒内移动到特定形状并最小化所有原子间相互作用的排斥力的。
为了理解蛋白质的工作原理并防止错误折叠,科学家们需要一种预测蛋白质折叠方式的方法,但解决这个难题并非易事。
2003年,华盛顿大学生物化学家大卫·贝克写了罗塞塔一个设计蛋白质的计算机程序。用它他证明了可以逆转蛋白质折叠问题。设计一个蛋白质结构然后进行预测创建它所需的氨基酸序列。
这是一个巨大的飞跃,但用于计算的形状很简单,而计算过程却非常复杂。要常规设计具有所需结构的新蛋白质,需要进行重大的范式转变。
机器学习的新时代
机器学习是一种人工智能类型,通过分析大量的数据,计算机学会解决各种问题。它已被应用于各个领域,从游戏玩耍以及语音识别到自动驾驶车辆以及科学研究机器学习的背后理念是利用数据中的隐藏模式来回答复杂问题。
这种方法在2010年当德米斯·哈萨比斯共同创立时取得了巨大的飞跃。深度思维一家旨在将神经科学与人工智能结合以解决现实世界问题的公司。
哈萨比斯在四岁的时候就因为是一名国际象棋神童而迅速引起了广泛关注。阿尔法零(AlphaZero),一个自学成才的国际象棋AI,在2017年击败了当时的世界顶级电脑国际象棋程序Stockfish-8。该AI能够从自己的游戏中学习,而不是依赖于预编程策略,这标志着人工智能世界的一个转折点。
不久之后,DeepMind将类似的技术应用于围棋,这是一种以极其复杂而著称的古老棋盘游戏。2016年,其人工智能程序阿尔法围棋击败了世界顶级选手李世石之一在游戏中让数百万观众震惊的备受关注的比赛.

2016年,哈萨比斯将深度思维的研究重点转向了一个新的挑战:蛋白质折叠问题。在领导下的约翰· jumper一位具有蛋白质科学背景的化学家开始了AlphaFold项目。团队使用一个包含实验确定的蛋白质结构的大数据库来训练人工智能,使其能够学习蛋白质折叠的原则。结果是AlphaFold2一个能够从氨基酸序列精确预测蛋白质三维结构的人工智能。
这是一个重要的科学突破。AlphaFold 从此预测了超过 2亿种蛋白质的结构——基本上涵盖了迄今为止科学家们所测序的所有蛋白质。此庞大的蛋白质结构数据库现已免费提供,加速了生物学、医学和药物开发领域的研究。
设计蛋白质以对抗疾病
理解蛋白质如何折叠和功能对于设计新药物至关重要。酶,一种蛋白质,作为生化反应的催化剂,可以加速或调节这些过程。为了治疗癌症或糖尿病等疾病,研究人员通常会针对参与疾病途径的特定酶进行研究。通过预测蛋白质的形状,科学家们可以确定小分子(潜在的药物候选物)可能会与之结合的位置,这是药物开发的第一步。设计新药物.
2024年,DeepMind发布了AlphaFold3这是一个升级版的AlphaFold程序,不仅可以预测蛋白质的形状,还可以识别小分子的潜在结合位点。这一进展使得研究人员更容易设计出能够精确靶向特定蛋白质的药物。
谷歌收购了Deepmind据报道大约为2014年的五亿美元谷歌DeepMind现已启动一项新业务,同构实验室与制药公司合作,利用这些AlphaFold3预测进行真实世界中的药物开发。

大卫·贝克本人继续在蛋白质科学领域做出重要贡献。他领导的华盛顿大学团队开发了一种名为“的人工智能方法。家族范围内的幻觉“他们用来从头设计全新蛋白质。幻觉是新的模式——在这种情况下,是指蛋白质——这些新模式是合理的,意味着它们与AI训练数据中的模式相吻合。这些新蛋白质包括一种发光的酶,证明机器学习有助于创造新型合成蛋白质。这些AI工具为设计功能性酶和其他天然进化过程中不可能产生的蛋白质提供了新的途径。”
人工智能将推动研究的下一阶段 развития исследования на следующую стадию 请确认您希望的内容是“人工智能将推动研究的下一阶段”,因为原始文本中提供的指令要求直接翻译,而给定的俄文句子似乎不是原文的有效翻译。根据您的需求,如果需要准确反映原句意思,请参考:“人工智能将开启研究的下一个篇章”。
哈萨比斯、贾姆珀和贝克的获奖成就表明,机器学习不仅是计算机科学家的工具——它现在已成为生物学和医学未来的重要组成部分。
通过解决生物学中最难的问题,2024年获奖者在药物发现、个性化医疗甚至对我们自身生命化学的理解方面开辟了新的可能性。

